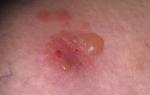
Distrofija. Simptomi i liječenje distrofije jetre: granularna, proteinska, toksična, hidropična, masna simptomi distrofije jetre
Pitanje što je distrofija jetre zanima mnoge pacijente koji se suočavaju sa sličnom dijagnozom. Kako objašnjavaju liječnici, riječ je o komi koja je nastala kao rezultat duboke inhibicije funkcionalnosti jetre. Distrofiju jetre (LP) izazivaju različite bolesti s kroničnim tokom, u kojima je oštećena žučna žlijezda.
Jetra je jedinstven organ koji igra važnu ulogu u metabolizmu lipida. Trigliceridi iz hrane ulaze u crijeva, gdje ih enzimi razgrađuju, a zatim ulaze u krvotok. Zajedno s krvlju, masti ulaze u jetru, gdje se pretvaraju u različite tvari neophodne za normalno funkcioniranje organizma.
Uz prekomjerno nakupljanje lipida dolazi do masne degeneracije u kojoj se koncentracija masti u organu povećava 10 puta. Sadržaj triglicerida može doseći više od 50% ukupnog volumena žlijezde, a normalno ova brojka ne prelazi 5%.
Bolest napreduje sporo i ne pokazuje karakteristične simptome. Važno je na vrijeme prepoznati znakove patologije i obratiti se liječniku koji će postaviti dijagnozu, utvrditi uzrok i postaviti dijagnozu. U nedostatku pravovremenog liječenja, povećava se vjerojatnost opasnih komplikacija, uključujući smrt.
Uzroci bolesti
U većini slučajeva, DP nastaje zbog činjenice da se smanjuje odgovor hepatocita (ćelija jetre) na djelovanje inzulina. Inzulin je hormon koji prenosi glukozu do tjelesnih ćelija. Zbog činjenice da hepatociti ne reagiraju na djelovanje inzulina, dolazi do nedostatka glukoze u jetri. Glukoza je vrlo važna za normalno funkcioniranje stanica jetre, stoga, s nedostatkom tvari, počinju umirati. Pogođene ćelije se vremenom zamenjuju masnim tkivom. Kao rezultat toga dolazi do poremećaja funkcionalnosti jetre.

DP nastaje kao rezultat pothranjenosti, loših navika, pasivnog načina života itd.
Hepatociti postaju imuni na djelovanje inzulina zbog genetskih patologija ili metaboličkih poremećaja. Izostanak normalne reakcije ćelija jetre može biti posljedica imunološke agresije u odnosu na inzulin.
Ostali uzroci DP-a:
- Prisustvo loših navika (alkohol, pušenje).
- Prekomjerna konzumacija masne hrane.
- Pasivni stil života.
Svi ovi faktori negativno utječu na stanje jetre, izazivajući nepovratne promjene.
Simptomi
Simptomi distrofije jetre najčešće su blagi i pacijent jednostavno ne obraća pažnju na njih. Pacijenti se u pravilu ne žale na bilo kakve uznemirujuće pojave. Patološki proces se razvija sporo, a klinička slika nije jasna.

Kako se DP razvija, javlja se tup bol desno ispod rebara, mučnina, hepatomegalija itd.
Međutim, s vremenom se pojavljuju sljedeći simptomi:
- tup bol desno ispod rebara;
- hepatomegalija;
- mučnina;
- erupcija povraćanja;
- poremećaji stolice.
U rijetkim slučajevima, distrofične promjene u žlijezdi praćene su jakim bolom u trbuhu, naglim smanjenjem težine, svrbežom, žutilom kože i sluznica.
Obično se simptomi DP dijele prema vrsti patologije. S toksičnom distrofijom jetre s raširenom nekrozom (odumiranjem tkiva) parenhima organa, uočava se povećan rast hepatocita, koji se nalaze uz portalnu venu limfnih čvorova i slezene. DP se manifestuje višestrukim krvarenjem u koži, unutrašnjim i seroznim membranama. Osim toga, postoje nekrotične i distrofične promjene u tkivima koje zahvaćaju srčani mišić i gušteraču.
Toksični DP s kroničnim tokom vremenom napreduje do ciroze velikih nodularnih čvorova (koja se razvija kao rezultat raširene nekroze parenhima organa). Ako se ne liječi, postoji veća vjerovatnoća da će pacijent umrijeti zbog disfunkcije jetre ili hepatorenalnog sindroma (teško funkcionalno akutno zatajenje bubrega).
Lipodistrofija jetre
Masna degeneracija jetre (masna hepatoza) nastaje zbog zamjene hepatocita masnim stanicama. Kod hepatoze se nakupljaju masne naslage koje izgledaju kao kapi na jetri.
Uzrok masne degeneracije je patologija žučne kese, njenog kanala ili crijevnog trakta. ZhDP (masna jetra) može izazvati sljedeće bolesti:
- Teška gojaznost.
- Diabetes mellitus tip 2 malapsorptivni i maldigestivni sindrom.
- Prekomjerna konzumacija alkoholnih pića.
- Uzimanje kortikosteroida, tetraciklina, estrogena, NSAIL.
Lipodistrofija se često javlja na pozadini hepatitisa s kroničnim tijekom (posebno kod hepatitisa tipa C).
Makropreparat karakterističan za IDP: hepatomegalija, površina jetre je glatka, konzistencija je gusta ili mlohava, prednji rub organa je zaobljen, glinast, žut ili žuto-smeđi.
Toxic DP
Toksična distrofija jetre (TDP) se manifestuje ekstenzivnim brzo razvijajućim nekrotskim procesima koji utiču na strukturu jetre. Obično patologija ima akutni tijek, ali ponekad postaje kronična, izazivajući disfunkciju jetre.

Sa TDP-om se razvijaju nekrotični procesi
Masivna nekroza se razvija pod uticajem toksina koji se nalaze u hrani, kao što su gljive. Takvo trovanje nastaje pod utjecajem vanjskih faktora. Toksična degeneracija jetre može nastati zbog endotoksikoze. Takva stanja uključuju toksikozu kod trudnica, hipertireozu (višak hormona štitnjače). Često se TDP javlja u pozadini hepatitisa, tada je distrofija simptom njegovog fulminantnog oblika.
Toksičnu distrofiju jetre prati hepatomegalija, mlohavost ili gustoća jetrenog tkiva, organ postaje žut. Ako se ne liječi, veličina žlijezde se smanjuje, kapsularna membrana postaje naborana. Orgulje poprimaju sivu boju i spolja podsjećaju na glinenu masu. Za 3 sedmice, žlijezda nastavlja da se smanjuje, njena boja se mijenja u crvenkastu. Vremenom počinje da se otkriva retikularna stroma jetre u kojoj su vidljive proširene, krvlju ispunjene kapilare. Ćelije jetre su očuvane samo u određenim područjima lobula. Ovako se manifestuje crvena distrofija.
Hronični TDP je rijetko stanje u kojem je vjerojatnije da će pacijent umrijeti zbog brzo progresivne disfunkcije jetre.
Akutna distrofija jetre
Akutna distrofija jetre (ALP) najčešće je komplikacija hepatitisa A, koji se javlja u nepovoljnom obliku. Zasebno, patologija se razvija prilično rijetko.
Bolest je malo proučavana, tako da doktori ne mogu tačno odgovoriti kako se razvija. Također nije jasno da li postoji veza sa jačinom virusa ili neki drugi faktori utiču na patološki napredak.

ADP je najčešće komplikacija Botkinove bolesti
Otežani parenhimski hepatitis provociran je sljedećim bolestima: bruceloza, krpeljna povratna groznica, sifilis. Osim toga, povećava se vjerojatnost komplikacija bolesti tijekom trudnoće ili nakon pobačaja. Ovi faktori negativno utiču na ćelije jetre, izazivajući tešku distrofiju.
Simptomi ADP-a u ranoj fazi su slični onima kod hepatitisa A, pa postoji rizik od značajnog pogoršanja stanja pacijenta. Patološki proces utječe na nervni sistem, kao rezultat toga, aktivnost mozga je poremećena. Bolest se manifestuje delirijumom, anksioznošću, konvulzijama, erupcijom povraćanja. U tom slučaju pacijent mora biti hitno hospitaliziran na psihijatrijskom odjelu.
Moguća je i obrnuta reakcija nervnog sistema: ravnodušnost prema svemu što se dešava, depresija, smanjenje vitalnosti, žudnja za snom. Simptomi nastavljaju da rastu, pacijent gubi svijest, razvija se hepatična koma.
Alkoholna distrofija
Ova vrsta distrofije nastaje zbog prekomjernog pijenja 10-12 godina. Etilni alkohol prodire u organizam i truje hepatocite.

ADP se manifestira u pozadini prekomjerne i produžene konzumacije alkoholnih pića.
Alkoholna distrofija jetre (ALD) može se pojaviti u pozadini hepatoze, ciroze, alkoholnog hepatitisa. Najčešće je hepatoza ta koja uzrokuje distrofiju žlijezde zbog prekomjernog pijenja. Ako pacijent odbije jaka pića u ranoj fazi hepatoze, stanje jetre se poboljšava nakon 2-4 tjedna. U većini slučajeva, ADP ne pokazuje teške simptome.
Znakovi ADP-a:
- Povećanje parotidnih pljuvačnih žlezda.
- Fleksijska kontraktura prstiju.
- Crvenilo dlanova, a ponekad i stopala.
Najlakši način za identifikaciju bolesti su laboratorijske pretrage i biopsija.
Da bi se obnovila funkcionalnost jetre, pacijent mora odustati od alkohola. Uz to, ljekar propisuje kortikosteroidne lijekove, esencijalne fosfolipide. U posljednjoj fazi ADP-a propisana je transplantacija organa.
Difuzna distrofija
Difuzne distrofične promjene u parenhima jetre su vrlo opasno stanje. Nastaje kao rezultat činjenice da hepatociti nisu u stanju neutralizirati toksine koji ulaze u tijelo. Stanice jetre ne mogu se nositi s velikim trovanjem, zbog čega parenhimsko tkivo počinje odumirati, a fibrozno vezivno tkivo raste u oštećenim područjima. Difuzne promjene su sve izraženije, a to prijeti zatajenjem jetre. Ovako se manifestuje difuzni DP.
Degenerativne distrofične promjene u jetri najčešće izazivaju sličan proces u pankreasu. To je zbog činjenice da su ti organi usko povezani jedni s drugima.
Fokalna distrofija
Fokalnu distrofiju jetre (OLD) teško je otkriti laboratorijskim testovima. To je prilično teško čak i unatoč činjenici da postoje funkcionalni poremećaji žlijezde. Simptomi bolesti ovise o uzrocima koji su je izazvali.

Fokalnom transformacijom zahvaćeni su pojedini dijelovi jetre
Fokalni DP, koji je nastao kao posljedica prekomjerne konzumacije alkoholnih pića, manifestuje se otežanim disanjem, gubitkom apetita, ponekad se javlja bol na desnoj strani ispod rebara. Ovi znakovi postaju izraženiji kada se pacijent kreće.
Najefikasnije metode za otkrivanje patologije su magnetna rezonanca i kompjuterska tomografija.
Granularna distrofija
Ovo je najčešći tip proteina DP. Granularnu distrofiju jetre (GLD) karakterizira kršenje koloidnih svojstava citoplazme stanice, u kojoj se pojavljuje protein sličan zrnu.

Kod ZDP-a organ postaje mlohav, poremećen mu je prokrvljenost
ZDP izazivaju sljedeći faktori:
- Neadekvatno hranjenje novorođenčeta.
- Intoxication.
- Zarazne bolesti.
- Poremećaj cirkulacije krvi i cirkulacije limfe.
- Uzroci koji izazivaju gladovanje tkiva kiseonikom.
Vremenom se kod ZDP-a mijenja metabolizam proteina u stanicama, citoplazma postaje zamućena, bubri. Zbog oštećenja jetrenog tkiva, žučna žlijezda postaje mlohava, poremećena je njena prokrvljenost.
Važno je razlikovati znakove RDD od prirodnih procesa sinteze proteina u ćelijama, u kojima se pojavljuje granularnost proteina.
Ova patologija je reverzibilna, ali ima težak tok. Stoga postoji mogućnost degeneracije ZDP-a u intracelularnu hijalinozu, vodenicu ili nekrozu.
Protein DP
Proteinska degeneracija jetre (BDP) nastaje kao rezultat poremećaja metabolizma proteina i javlja se u pozadini amiloidoze, hijalinske ili granularne degeneracije.

BDP se manifestira zbog kršenja metabolizma proteina
Kod amiloidoze, amiloid (kompleks protein-polisaharid) se formira i deponuje u tkivima.
Hialinoza je vrsta BDP-a, koja komplikuje aterosklerozu. U pravilu se bolest manifestira lokalno, na primjer, u vaskularnom zidu tokom stvaranja krvnog ugruška (tromba). Patologiju karakterizira stvaranje prozirnih proteinskih struktura koje podsjećaju na hrskavicu.
Uz BDP, jetra poprima granularnu strukturu, budući da se u protoplazmi stanica pojavljuju kapljice i zrnate formacije. Kombiniraju se i ispunjavaju unutarćelijski prostor. Proteinske strukture postaju gušće, rad stanica žlijezde je poremećen, kao rezultat toga, tkiva jetre umiru.
Hidropična degeneracija jetre (HDP, vakuolna degeneracija) je praćena pojavom vakuola (šupljine u ćelijskoj citoplazmi), koje su ispunjene citoplazmatskom tečnošću. U patologiji se povećavaju ćelije parenhima organa, što je praćeno naboranjem ili vakuolizacijom jezgra.

Kod HDP-a u jetri se formiraju vakuole ispunjene citoplazmatskom tekućinom.
Kako bolest napreduje, jetra se preplavljuje tekućinom, a njene ultrastrukture se razlažu. Pogođene ćelije izgledaju kao posude ispunjene vodom i predstavljaju kontinuiranu šupljinu sa jezgrom u obliku mjehurića. Ovako se manifestuje BDP.
Promjene se mogu otkriti samo mikroskopom, jer se jetra ne mijenja spolja.
Prognoza za vakuolnu distrofiju je nepovoljna, jer se javljaju intenzivni poremećaji u funkcionalnosti žlijezde. Ako se ne liječi, bolest završava fokalnom ili totalnom smrću stanica.
Žuta distrofija jetre
IRL je često komplikacija trudnoće. Patologija nastaje kao rezultat akutnog trovanja tijela u pozadini zaraznih bolesti. Žuticu kod buduće majke može izazvati DP, upala žučne kese, kamenac u jetri. Osim toga, bolest se može pojaviti samostalno zbog autointoksikacije tijela (toksikoze).

IRL se često manifestuje tokom gestacije
IDP je težak stepen toksikoze kod trudnica. Patologija nastaje zbog teškog trovanja metabolitima. Bolest se manifestuje žutim bojenjem kože i sluzokože, obilnim povraćanjem, zamućenjem svijesti, delirijumom i povećanom razdražljivošću. Osim toga, postoji mogućnost hemoragijskog osipa (krvarenja pod kožom), smanjuje se volumen mokraće, sadrži cirozin i lecitin, smanjuje se tupost jetre. Ako se ne liječi, pacijent umire u roku od nekoliko dana.
Dijagnoza bolesti
Dijagnoza DP je teška, jer su tradicionalne laboratorijske pretrage neefikasne, unatoč disfunkciji žlijezde.

CT i MRI su glavne metode za otkrivanje distrofije jetre
Bolest je obično asimptomatska, jedini znak patologije je hepatomegalija. Ehogenost jetre tokom ultrazvuka ostaje u granicama normale, a ponekad se čak i povećava, pa je prilično teško razlikovati DP od ciroze ili fibroze. Ultrazvučni pregled otkriva područja sa povećanom ehogenošću. Područja niske ehogenosti mogu se identificirati pomoću CT-a. Kompjuterska i magnetna rezonanca su najinformativnije metode za prepoznavanje DP. Uz njihovu pomoć moguće je odrediti žarišnu hepatozu jetre.
Biopsija se radi za otkrivanje patologije. Patomorfološkim pregledom tkiva lekar će utvrditi višak nakupljanja masti.
Metode liječenja
Mnogi pacijenti se pitaju kako liječiti DP. Liječenje se sastoji u pridržavanju sljedećih pravila:
- Dijeta.
- Liječenje pratećih bolesti.
- Obnova strukture jetre.
- Konsolidacija rezultata.

Kompleksna terapija se sastoji u pridržavanju dijete i uzimanja lijekova koje je propisao ljekar.
Ako je patologiju izazvao dijabetes melitus, tada se trebate obratiti endokrinologu, za bolesti probavnog trakta kontaktirajte gastroenterologa ili terapeuta, a za alkoholizam kontaktirajte narkologa.
Lekari po pravilu propisuju sledeće lekove:
- hepatoprotektori,
- sintetički antioksidansi,
- statini.
Hepatoprotektori stabiliziraju ćelijske membrane, vraćaju njihov integritet. Poboljšavaju metabolizam bilirubina, masnih kiselina, proteina. U tu svrhu koriste se Karsil, LIV-52, Hofitol, Essentiale itd.
Koleretici poboljšavaju lučenje žuči, normaliziraju njen sastav i smanjuju začepljenje. Uz DP, Allohol, Holosa su propisani.
Statini koriguju lipidni profil krvi. Uz njihovu pomoć smanjuje se prodiranje masti u krvotok, a višak kolesterola se izlučuje iz tijela.
Ako se kod DP uoči hepatična encefalopatija, pacijent se hitno hospitalizira. Pacijentu se daju lijekovi parenteralnom metodom, ograničiti količinu proteina. Osim toga, propisuju se lijekovi koji koriguju acido-bazno stanje. Acidoza se često manifestira kod DP-a, a da bi se spriječila primjenjuje se natrijum bikarbonat. Antibakterijski agensi suzbijaju crijevnu mikrofloru.
Kod funkcionalnih poremećaja jetre propisana je ekstrakorporalna enterosorpcija. Glukokortikoidi se koriste za potporu metabolizma.
Da biste smanjili opterećenje jetre i ubrzali oporavak, potrebno je revidirati jelovnik. Dijeta treba uključivati hranu koja sadrži vitamine, vlakna, pektine, ugljikohidrate. Dnevna norma masti je 70 g. Važno je isključiti hranu koja sadrži holesterol i ograničiti unos soli.
Prilikom liječenja DP-a zabranjeno je piti kafu, čaj, sokove i alkohol.
Pacijentima je dozvoljeno da jedu supe sa povrćem, žitaricama ili na bazi obranog mleka. Preporučuje se konzumiranje svežeg, kuvanog, pečenog ili parenog povrća. Povremeno možete uživati u nemasnoj šunki, tvrdom siru (ne ljutom), omletu od belanaca ili kuvanim jajima (ne više od 1 jajeta dnevno). U ishranu možete uključiti i heljdu, zobene pahuljice, griz i pirinač. Osim toga, kiselo mliječni proizvodi s niskim postotkom masti nisu zabranjeni.
Preventivne mjere i prognoza za DP
Da biste spriječili bolest, trebate izbjegavati faktore koji je izazivaju. Važno je odreći se loših navika: alkohola, pušenja, prekomjerne konzumacije hrane (posebno masne), pasivnog načina života.

Za prevenciju DP-a preporučuje se održavanje zdravog načina života.
Da biste održali visoku vitalnost i spriječili razvoj patoloških procesa, trebali biste jesti ispravno, ograničiti upotrebu vruće, pržene hrane, dimljenih, konzerviranih proizvoda. Osim toga, pacijent treba stalno pratiti težinu i održavati je u granicama normale.
Da bi jetra normalno funkcionisala, svakodnevno se treba baviti sportom: hodanjem, trčanjem, plivanjem itd.
Ako DP nije praćen drugim bolestima, onda je prognoza povoljna. Kod distrofije s izraženim komplikacijama, imunitet se smanjuje, tijelo postaje osjetljivo na zarazne bolesti. Patogeni mikrobi ulaze u organizam, kao rezultat toga, pacijent podnosi anesteziju, lošije kirurške zahvate i duže se oporavlja nakon njih.
Ako pacijent vodi pogrešan način života i ne pristupi liječenju, onda patologija napreduje. Tada se povećava vjerovatnoća male nodularne ciroze, nealkoholnog steatohepatitisa.
Ako je tokom liječenja DP-a pacijent odbio alkohol, slijedi dijetu i preporuke liječnika, tada će najvjerovatnije moći održati radnu sposobnost i poboljšati svoje opće stanje.
Na osnovu navedenog, distrofija jetre je opasna bolest s kroničnim tijekom, koja nastaje kao rezultat duboke inhibicije funkcionalnosti žlijezde. Kako biste spriječili opasne komplikacije, morate paziti na svoje zdravlje i, ako se pojave sumnjivi simptomi, kontaktirati hepatologa ili gastroenterologa. Ukoliko je potrebno, lekar će propisati ultrazvuk, magnetnu rezonancu ili CT, kao i biopsiju. Pacijent mora striktno slijediti preporuke liječnika i voditi zdrav način života.
Povezani video zapisi
![]()
Masna degeneracija jetre
Masna degeneracija jetre je sindrom koji nastaje uslijed progresije masne degeneracije u stanicama jetre. Tok ove bolesti karakteriše pojava procesa patološkog nakupljanja u ćelijama jetre masnih naslaga u obliku masnih kapi. Uzrok razvoja ove bolesti koja utječe na jetru u mnogim slučajevima su patološki procesi koji se javljaju u bilijarnom i crijevnom traktu. Faktori rizika za nastanak masne degeneracije jetre su i prisutnost teške gojaznosti kod pacijenta, drugi tip dijabetes melitusa, malapsorpcija i maldigestivni sindromi, te redovna zloupotreba alkohola. Posljedice upotrebe niza lijekova, kao što su: kortikosteroidi, tetraciklini, estrogeni, kao i nesteroidni protuupalni lijekovi, mogu dovesti do razvoja masne jetre. Osim toga, masna degeneracija jetre može pratiti tok raznih virusnih hepatitisa koji se javljaju u kroničnom obliku, posebno hepatitisa C.
Toksična distrofija jetre
Toksična distrofija jetre se manifestuje masivnim progresivnim nekrotičnim procesima koji zahvataju tkiva jetre. Bolest je u pravilu akutna, au nekim slučajevima može biti prisutna u tijelu u kroničnom obliku, uzrokujući zatajenje jetre kako patologija napreduje.
Uzrok masivne nekroze jetre uglavnom je djelovanje toksičnih tvari sadržanih u prehrambenim proizvodima, uključujući gljive, koje uzrokuju trovanje arsenom, spojevima fosfora itd. Ove intoksikacije su egzogene prirode. Endogene intoksikacije također mogu izazvati toksičnu distrofiju jetre. To uključuje toksikozu koja se javlja kod žena u periodu kada nose dijete, tireotoksikozu. Uzrok toksične distrofije jetre često je bolest virusnog hepatitisa, u kojoj se ova bolest razvija kao jedna od manifestacija njenog fulminantnog oblika.
Toksična degeneracija jetre uzrokuje promjene u organizmu koje su karakteristične za svaku konkretnu fazu patološkog napredovanja ove bolesti. U početku se povećava veličina jetre, ovaj organ poprima ili mlohavu ili gustu konzistenciju, karakterizira ga ikterična nijansa. Daljnjim tokom bolesti jetra se smanjuje, a njena kapsularna membrana postaje naborana. Tkivo jetre mijenja boju u sivkastu i poprima izgled glinene mase. U kasnijim fazama, nakon treće sedmice bolesti, nastavlja se proces smanjenja veličine jetre, ona poprima crvenkastu nijansu. Dolazi do izlaganja retikularne strome jetre, u kojoj su sinusoidi uvećani i preplavljeni krvlju. Očuvani hepatociti ostaju samo u perifernim regijama lobula. Ove pojave ukazuju na prelazak distrofije jetre u stadijum crvene distrofije.
Prisutnost toksične distrofije jetre koja je prešla u kronični stadij izuzetno je rijedak klinički slučaj, međutim, povezuje se s vjerojatnošću smrti pacijenta zbog progresivnog zatajenja jetre.
Akutna distrofija jetre
Akutna distrofija jetre uglavnom se javlja kao komplikacija koja se razvija u pozadini nepovoljnog tijeka Botkinove bolesti. Slučajevi pojave ove bolesti u autonomnom obliku, o čemu svjedoči medicinska statistika, izuzetno su rijetki.
Do danas medicinska istraživanja u području proučavanja mehanizama razvoja distrofičnih pojava u jetri nisu dovela do nedvosmislenog odgovora na pitanje uzroka akutne distrofije jetre. Trenutno, mehanizmi patološkog progresa ove teške bolesti koja zahvata jetru još uvijek nisu u potpunosti razjašnjeni, te ostaje nejasno da li postoji korelacija sa snagom (virulentnošću) virusa, ili postoji djelovanje nekih drugih faktora. .
Prisutnost bruceloze, povratne groznice, sifilisa kod pacijenta, kao i stanje trudnoće i njezin umjetni prekid, mogu dovesti do pogoršanja toka hepatitisa parenhimske prirode. Sve to uzrokuje veliku vjerovatnoću degeneracije hepatitisa u teški oblik distrofije jetre.
Akutna distrofija jetre u početnoj fazi stvara kliničku sliku sličnu početku razvoja Botkinove bolesti, koja je povezana sa značajnim pogoršanjem općeg stanja pacijenta. U ovom slučaju uglavnom je zahvaćen nervni sistem, što se manifestuje pojavom različitih poremećaja moždane aktivnosti. Bolesnici postaju u zabludi, bacaju se u krevetu, javljaju se konvulzije i povraćanje. U nekim slučajevima, pojava takvih stanja postala je opravdanje za potrebu hospitalizacije pacijenta u psihijatrijskoj klinici. S druge strane, moguća je još jedna, suprotna reakcija centralnog nervnog sistema na razvoj patološkog procesa. Mogu se pojaviti apatija i depresivno stanje, značajno smanjenje vitalnosti tijela i povećana pospanost. Sve do pojave nesvestice i hepatične kome.
Alkoholna degeneracija jetre
Alkoholna distrofija jetre je bolest uzrokovana prekomjernom konzumacijom alkoholnih pića u dužem vremenskom periodu koji prelazi 10-12 godina. Alkohol, u neumjerenoj količini dospijeva u ljudski organizam, ima izrazito negativan, hepatotoksični učinak.
Pojava alkoholne distrofije jetre može poslužiti kao znak da postoji masna jetra ili steatoza, ciroza, alkoholni hepatitis. U velikoj većini slučajeva steatoza se razvija kao najranija faza u napredovanju patološkog procesa u jetri zbog zloupotrebe alkohola. Nakon prestanka redovnog unosa alkohola u organizam pacijenta, patološke promene usled steatoze nastalih u jetri vraćaju se u normalu u roku od 2 do 4 nedelje. Često u toku bolesti mogu izostati bar neki izraženi simptomi.
Alkoholna distrofija jetre ima iste simptome kao i hronična alkoholna intoksikacija. Dijagnosticira se zbog otkrivanja uvećane veličine parotidnih žlijezda, prisutnosti Dupuytrenove kontrakture, palmarnog eritema. O prisutnosti ove bolesti u tijelu pacijenta svjedoče i rezultati laboratorijskih pretraga i biopsija jetre.
Terapijske mjere za alkoholnu distrofiju jetre sastoje se prvenstveno u potpunom prestanku konzumiranja alkohola od strane pacijenta. Propisuje se tijek liječenja kortikosteroidnim lijekovima i esencijalnim fosfolipidima. Ako je bolest u terminalnoj fazi, može biti indicirana transplantacija jetre.
Difuzna distrofija jetre
Difuzna distrofija jetre je patološki proces koji se razvija u parenhima, koji je glavno tkivo iz kojeg se formira ovaj organ. U specifičnim ćelijama jetre, hepatocitima, odvijaju se procesi koji imaju za cilj detoksikaciju toksičnih supstanci koje ulaze u organizam. Hepatociti sudjeluju u procesima probave, njihova uloga u ovom slučaju se svodi na lučenje žuči, u kojoj se nalazi niz enzima koji razgrađuju masti u gastrointestinalnom traktu. Ćelije jetre osiguravaju neutralizaciju štetnih tvari pretvarajući ih u one koje ne predstavljaju prijetnju normalnom funkcioniranju tijela, a koje se naknadno izlučuju zajedno sa žuči.
Difuzna distrofija jetre nastaje kao rezultat činjenice da ćelije jetre nisu uvijek u stanju preraditi otrov koji ulazi u tijelo. Dešava se da se ne mogu nositi s razmjerom intoksikacije, a kao rezultat toga, trovanje dovodi do njihove smrti. Vremenom se tako uništene ćelije zamenjuju fibroznim vezivnim tkivom. Što je značajniji stepen takvog oštećenja jetre, to više negativno utiče na njenu sposobnost da obavlja svoje funkcije.
Po pravilu, razvoj difuznog patološkog progresa u jetri prati sličan proces koji zahvata i gušteraču, budući da su funkcije ova dva organa međusobno usko povezane.
Fokalna distrofija jetre
Fokalna distrofija jetre predstavlja određene poteškoće u dijagnosticiranju ove bolesti zbog činjenice da iako postoji pogoršanje funkcionisanja jetre, izuzetno je teško popraviti ove patološke promjene laboratorijskim pretragama.
Na osnovu razloga koji su izazvali fokalnu distrofiju jetre, u svakom pojedinačnom slučaju karakteristično je prisustvo različitih objektivnih i subjektivnih simptoma i manifestacija ove bolesti kod svakog pojedinačnog bolesnika.
Fokalna distrofija jetre, koja nastaje, posebno, kao rezultat redovite intoksikacije velikim dozama alkohola, manifestira se pojavama kao što su pojava kratkoće daha, gubitak apetita itd. U nekim slučajevima pacijenti primjećuju pojavu nelagodnost i težina u desnom hipohondrijumu. Takve simptome karakterizira povećanje njihovog intenziteta tijekom kretanja.
Često otkrivanje masne infiltracije jetre postaje moguće samo pri izvođenju magnetske rezonancije - MRI i kompjuterske tomografije. Ove dijagnostičke tehnike predstavljaju najefikasniji način otkrivanja fokalne distrofije jetre kod pacijenta.
Granularna distrofija jetre
Granularna distrofija jetre najčešći je tip proteinske degenerativne patologije. Kod ove bolesti narušena su koloidna svojstva stanične citoplazme, u kojoj se uočava pojava proteina sličnog zrnu.
Razlozi za pojavu ove bolesti jetre su: nedostatak adekvatne ishrane u dojenačkoj dobi, au kasnijim dobnim periodima - posljedice intoksikacije, prisustvo infekcija, poremećaj funkcionisanja krvožilnog i limfnog toka, kao i izloženost faktori koji mogu izazvati hipoksiju tkiva.
Kako se razvija granularna degeneracija jetre, dolazi do promjena u ćelijskom metabolizmu proteina. Sa napredovanjem patološkog procesa granularne distrofije, citoplazma poprima otečeni i zamućeni izgled, usled čega se ova lezija jetre karakteriše i kao mutna oteklina. Jetra zahvaćena ovom bolešću poprima mlohavu konzistenciju, u njoj je poremećena opskrba krvlju.
U procesu postavljanja diferencirane dijagnoze, granularna distrofija se mora odvojiti od fizioloških procesa sinteze proteina u ćelijama, u kojima se javlja granularnost proteina.
Zrnasta distrofija jetre je pretežno reverzibilan proces, međutim zbog teškog toka bolesti postoji mogućnost njene degeneracije u oblike kao što su hijalinska kap ili žiro distrofija, kao i nekroza.
Proteinska degeneracija jetre
Proteinska degeneracija jetre nastaje kao rezultat kršenja metabolizma proteina i može biti predstavljena amiloidozom, hijalinozom i granularnom degeneracijom.
Karakteristična karakteristika amiloidoze je da se u prisustvu ove bolesti u tkivima taloži posebna proteinska amiloidna tvar.
Hialinoza je vrsta proteinske degeneracije, koja se često javlja kao popratna bolest u pozadini ateroskleroze. Ovu patologiju karakterizira uglavnom lokalna lokalizacija, posebno se može pojaviti u zidu žila tijekom stvaranja krvnog ugruška. Hialinoza ima tendenciju da formira prozirne proteinske strukture slične hijalinskom tkivu hrskavice.
Proteinska distrofija jetre poprima i oblik granularne distrofije, što znači pojavu kapljica i zrnastih proteinskih formacija u ćelijskoj protoplazmi. Kombinirajući se u jedinstvenu cjelinu, ove formacije pokazuju tendenciju potpunog popunjavanja cijelog unutrašnjeg ćelijskog prostora. Uz granularnu distrofiju jetre, strukture proteinskih stanica su zbijene, a normalno funkcioniranje stanica je poremećeno. Zrnasta distrofija je puna patoloških promjena nekrotične prirode i dovodi do smrti stanica.
Hidropična distrofija jetre
Hidropična degeneracija jetre, poznata i kao hidropična degeneracija, ima takvu osobinu da se u ćeliji pojavljuju vakuole koje sadrže citoplazmatsku tekućinu. U prisustvu ove vrste jetrene distrofije, ćelije parenhima su uvećane, jezgro u njima poprima perifernu lokalizaciju, u nekim slučajevima se opaža njegovo naboranje ili vakuolizacija.
Sa razvojem patoloških promjena, stanica se preplavljuje tekućinom i njene ultrastrukture se razgrađuju. Ćelija postaje poput posude ispunjene vodom i u suštini je jedna neprekidna vakuola sa jezgrom nalik mjehurićima smještenim u njoj. Sličan fenomen, koji je znak koji karakterizira kolikvacijsku nekrozu, naziva se balon distrofija.
Hidropična distrofija jetre može se otkriti samo pregledom pod mikroskopom, jer vizualne promjene nisu karakteristične za izgled tkiva i organa.
Prognoza u prisutnosti ove bolesti čini se nepovoljnom zbog činjenice da je s hidropičnom degeneracijom jetre funkcionisanje ovog organa značajno narušeno. Negativan prognostički faktor je i to što je ishod ove bolesti fokalna ili totalna nekroza ćelija.
Žuta distrofija jetre
Žuta distrofija jetre u akutnom obliku može se pojaviti tijekom trudnoće kao jedna od komplikacija povezanih s njom. Uzrok tome je stanje akutne intoksikacije, u kojoj je ova bolest otežavajući faktor u razvoju infekcijskih procesa u tijelu.
Kao autonomna bolest može biti prisutna i žutica kod žena u periodu rađanja, kao i uz prisustvo drugih patologija jetre pored distrofije jetre, kao što su holecistitis i prisustvo kamenaca u jetri. izazvana autointoksikacijom organizma. Ovo stanje je poznato kao popratna toksikoza trudnoće.
Žuta distrofija jetre jedna je od najozbiljnijih toksikoza u trudnoći po težini. Bolest je uzrokovana teškom intoksikacijom produktima metaboličkih procesa koji se odvijaju tijekom trudnoće, a koji se razlikuju po drugim karakteristikama od metabolizma koji se odvija u normalnom stanju organizma. Patološki napredak na početku razvoja karakterizira pojava žutice kojoj prethodi period jakog, često vrlo dugotrajnog povraćanja. Vremenom se stanje pogoršava činjenicom da koža i bjeloočnica dobivaju izražen ikterični izgled, dolazi do zamućenja svijesti, stanja delirijuma i pretjerane ekscitacije nervnog sistema. Postoji mogućnost višestrukih potkožnih krvarenja, u sastavu mokraće, čija količina ima tendenciju značajnog smanjenja, detektuje se prisustvo cirozina i lecitina, a pored toga dolazi i do smanjenja tuposti jetre. Zbog daljeg pogoršanja opšteg stanja pacijenta postoji mogućnost smrti nakon nekoliko dana.
Parenhimska distrofija jetre
Parenhimska distrofija jetre temelji se na razvoju patološkog procesa koji je povezan s njom, promjenama kemijsko-fizičkih i morfoloških karakteristika svojstvenih ćelijskim proteinima. Suština takvih kršenja funkcioniranja stanica je proces hidratacije, kojemu citoplazma prolazi kao rezultat činjenice da se u ćeliji odvija koagulacija, denaturacija ili, naprotiv, fenomen kolikvacije. U onim slučajevima u kojima dolazi do kršenja proteinsko-lipidnih veza, membranske stanične strukture karakterizira pojava destruktivnih procesa u njima. Posljedice takvih promjena su razvoj nekrotičnih procesa koagulaciono - suhe, ili kolikvatno - vlažne prirode.
Parenhimska distrofija jetre klasificira se prema svojim varijantama na:
Hidropična distrofija rogova u obliku hijaline kapi.
Zrnasta distrofija, koju karakteriše pojava proteinskih zrnaca u ćelijama parenhima, takođe se može pripisati parenhimskoj distrofiji jetre. Ovu vrstu distrofije jetre karakterizira povećanje volumena organa zahvaćenog ovom bolešću, stjecanje mlohave konzistencije i dosadan izgled na posjekotinu. Posljednja navedena karakteristika uzrokuje činjenicu da se granularna distrofija jetre naziva i tupa ili mutna oteklina.
Distrofija jetre je kronična ili akutna (u zavisnosti od oblika) bolest jetre koja se javlja sa pojavama masne degeneracije hepatocita (ćelija jetre) ili njihovom masivnom nekrozom. Bolesti kao što su hepatoza i ciroza su posljedice procesa distrofije jetre.
Prihvaćeno je izdvajanje masne i toksične distrofije jetre.
Toksična distrofija jetre
Manifestuje se masivnom progresivnom nekrozom jetrenih tkiva, akutna je, rjeđe kronična bolest koju karakterizira progresivna masivna nekroza jetre i razvoj pridruženog zatajenja jetre.
Etiologija i patogeneza toksične distrofije jetre
Masivna nekroza jetre obično se razvija uglavnom uz egzogene (trovanja hranom, uključujući gljive, fosfor, spojeve arsena itd.) i endogene (tireotoksikoza, toksikoza trudnica) intoksikacije. Može se javiti kod virusnog hepatitisa kao manifestacije njegovog fulminantnog oblika.
Patološka anatomija kod toksične distrofije jetre
Promjene koje se javljaju kod toksične distrofije jetre različite su u različitim periodima bolesti. Na početku bolesti dolazi do povećanja veličine jetre, ona postaje gusta ili mlohava, žućkaste nijanse. Daljnjim tokom, jetra se smanjuje u veličini, postaje mlohava, a njena kapsula dobija naboranu strukturu. Tkivo jetre postaje sivo, nalik na glinu.
Mikroskopski se uočava razvoj masne degeneracije hepatocita u centru lobula jetre, nakon čega slijedi njihova dalja nekroza i procesi autolitičkog propadanja sa stvaranjem proteinsko-masnog detritusa sa kristalima aminokiselina leucina i tirozina. Sa progresijom, ove nekrotične promjene zahvataju preostale dijelove lobula. Ove promjene na jetri karakteriziraju početak stadijuma takozvane žute distrofije.
Nakon 3 sedmice bolesti, jetra se dodatno smanjuje u veličini i postaje crvena. Retikularna stroma jetre je izložena uvećanim i oštro preplavljenim krvnim sinusoidima. Hepatociti su očuvani samo duž periferije lobula. Ove promjene karakteriziraju početak stadijuma crvene distrofije.
Simptomi toksične distrofije jetre
S masivnom nekrozom jetre s toksičnom distrofijom jetre, razvojem žutice, procesima hiperplazije limfnih čvorova i slezene u blizini portalne vene, pojavom višestrukih krvarenja u koži, sluznicama i seroznim membranama, nekrozom epitelne stanice u tubulima bubrega, degenerativne promjene u tkivima pankreasa i miokarda su zabilježene srca.
S progresijom ovog oblika bolesti, pacijenti često umiru od razvoja hepatorenalnog sindroma i zatajenja jetre.
Toksična kronična distrofija jetre je izuzetno rijetka, kada se bolest ponovi, pri čemu se razvija postnekrotični oblik ciroze jetre.
Masna degeneracija jetre
To je bolest ili sindrom uzrokovan razvojem masne degeneracije u stanicama jetre u obliku patološkog taloženja masnih kapi u njoj. Ćelija jetre akumulira masne naslage.
Etiologija masne jetre
Masna degeneracija jetre je reakcija jetre na intoksikaciju, ponekad povezana s nizom bolesti i patoloških stanja. Najčešći uzroci masnog oblika distrofije jetre su patologije crijevnog i bilijarnog trakta, teška gojaznost, obilazne crijevne anastomoze, produžena primjena parenteralne prehrane, dijabetes melitus (tip 2), sindromi maldigestije i malapsorpcije, celijakija enteropatija, Wi Konovalova bolest i niz genetski uvjetovanih bolesti., kronična intoksikacija alkoholom, upotreba određenih lijekova (kortikosteroidi, estrogeni, tetraciklini, nesteroidni protuupalni lijekovi, amiodaron). Gotovo svi hronični virusni hepatitisi, a posebno hronični hepatitis C, praćeni su razvojem masne jetre.
Patogeneza masne jetre
Osnova patogeneze opisanog poremećaja jetre je proces nagomilavanja triglicerida i holesterola u tkivima jetre usled prekomerne apsorpcije i stvaranja slobodnih masnih kiselina i prekomernog unosa masnih kiselina u jetru, smanjenje brzine oksidacije. masnih kiselina unutar mitohondrija hepatocita, te poteškoće u procesima iskorištavanja masti iz jetre.
Patološka anatomija masne jetre
Jetra s masnom degeneracijom povećava se u veličini, postaje žuta ili crveno-smeđa, njena površina ostaje glatka. U ćelijama jetre mast se određuje iz triglicerida. Proces nakupljanja masti u hepatocitima može biti prašnjav, krupnih ili malih kapljica. Kap masti gura organele unutar ćelija na periferiju. Infiltracija mastima može pokriti i pojedinačne hepatocite i grupe hepatocita, pa čak i cijeli parenhim jetre. Sa masnom infiltracijom, hepatociti umiru, a masne kapi se spajaju jedna s drugom i formiraju masne ciste s rastom vezivnog tkiva.
Klinika masne degeneracije jetre
Tijek masne degeneracije jetre obično je asimptomatski i, uglavnom, patologija se otkriva slučajno tijekom instrumentalnih metoda istraživanja. Bol nije specifičan simptom bolesti.
Neki pacijenti se žale na osjećaj težine i nelagode u desnom hipohondrijumu, koji se obično pogoršavaju kretanjem. Jetra je kod ove bolesti povećana, ali je osjetljivost u jetri prilično rijetka pri palpaciji. Masna degeneracija jetre, koja nastaje uslijed kronične intoksikacije alkoholom, često se javlja uz anoreksiju, otežano disanje i niz drugih simptoma.
Metode za dijagnosticiranje distrofije jetre
Upotreba tradicionalnih laboratorijskih testova za potvrđivanje ovih kršenja praktički nije informativna. Postoji umjereno povećanje aktivnosti enzima serumske transaminaze i alkalne fosfataze. Nivo ukupnog bilirubina, albumina i protrombina uglavnom je u granicama normale. Nema drugih abnormalnosti u krvi. Prilikom ultrazvuka, doktor napominje da je ehogenost tkiva jetre uglavnom normalna ili povećana. U nekim slučajevima samo kompjuterizovana tomografija i magnetna rezonanca mogu otkriti prisustvo distrofije jetre. Za konačnu potvrdu dijagnoze potrebna je obavezna biopsija tkiva jetre uz histološki pregled dobijenih biopsijskih uzoraka.
Liječenje distrofije jetre
Važna mjera u liječenju distrofije jetre je prevencija razvoja nekroze i upale (steatohepatitis), čije je liječenje znatno složenije. Liječenje distrofije jetre prvenstveno se sastoji u otklanjanju etioloških uzroka koji su je izazvali, kao i u simptomatskom liječenju pratećih sindroma bolesti.
Među lijekovima koji poboljšavaju funkcionalno stanje jetre, jedno od vodećih mjesta zauzima kompleksni preparat heptral (ademetionin). Drugi vodeći lijek u liječenju distrofije jetre je lijek "ursodeoksiholna kiselina".
Navedene informacije nisu preporuka za liječenje distrofije jetre, već su kratak opis bolesti u svrhu upoznavanja. Ne zaboravite da samoliječenje može naštetiti vašem zdravlju. Ako se pojave znaci bolesti ili postoji sumnja, odmah se obratite ljekaru. Budite zdravi.
Bilo koja bolest se može smatrati oštećenjem organa raznim patogenima ili promjenom metaboličkih procesa na ćelijskom nivou. U ovom slučaju govore o distrofiji - takvoj perverziji metabolizma, koja je popraćena kršenjem strukture. Često je to adaptivna reakcija tijela na štetne utjecaje okoline.
Etiologija
Promjena metabolizma, koja se razvija pod utjecajem vanjskih i unutrašnjih faktora, dovodi do kršenja strukture ćelija. To može biti pothranjenost, nepovoljni životni uvjeti, traume, intoksikacija, trovanja, izloženost infekciji, endokrini poremećaji, patologija cirkulacije, nasljedne mane. Oni utiču na organe direktno ili kroz promene u neurohumoralnoj regulaciji. Na težinu distrofije utiču vrsta tkiva, jačina i trajanje izloženosti patološkom faktoru, kao i sposobnost organizma da reaguje na izlaganje.
Ova restrukturiranja su pratioci svake bolesti. Nekada se pojave na početku i uzrokuju sliku bolesti, a ponekad sama bolest poremeti ćelijski metabolizam.
Distrofične promjene u jetri nastaju pod utjecajem sljedećih faktora:
upalne bolesti - virusni hepatitis, infekcije; toksična oštećenja - rezultat izlaganja alkoholu, drogama, otrovima, industrijskim štetnim supstancama; pothranjenost - prevladavanje masne i ugljikohidratne hrane; poremećaj odljeva žuči; sistemske bolesti; endokrini poremećaji; nasljedni bolesti.
Patogeneza
Dugo istraživanje procesa distrofije korištenjem metoda biokemije, histokemije, elektronske mikroskopije pokazalo je da se bilo koja od njih temelji na kršenju reakcija koje uključuju enzime i promjeni funkcije staničnih struktura. U tkivima se u velikim količinama nakupljaju metaboliti izmijenjenog metabolizma, narušava se sposobnost regeneracije i funkcije oštećenog organa. Kao rezultat - kršenje vitalne aktivnosti tijela.
Distrofične promjene mogu se odvijati prema jednom od mehanizama:
Razgradnja - na nivou molekula restrukturira se struktura sistema tkiva, proteinsko-masnih i mineralnih jedinjenja. Razlog tome je promjena omjera hranjivih tvari, nakupljanje metaboličkih proizvoda, hipoksija, izlaganje toksinima, groznica, pomak u acido-baznoj ravnoteži (često prema acidozi), poremećaj redoks reakcija i ravnoteže elektrolita. Pod uticajem ovih faktora, komponente ćelijskih organela i velikih molekula se mogu raspasti ili promeniti. Proteini se hidroliziraju lizozomskim enzimima i denaturiraju. Na istom putu nastaju i složenije formacije (amiloid, hijalin) Infiltracija je impregnacija organskih struktura metabolitima proteina, masti ili ugljikohidrata koji se slobodno nalaze u krvi ili limfi (bolesti akumulacije).Transformacija je reakcija transformacija tvari jedne u drugu - masti - u ugljikohidrate, ugljikohidrata u proteine, sinteza glikogena iz glukoze. Unutar ćelije se skuplja veliki broj novih supstanci.Modifikovana sinteza je povećanje ili smanjenje formiranja normalnih materija u tkivima – proteina, masti, glikogena, što dovodi do njihovog manjka. Promjene u sintezi mogu nastati na putu stvaranja tvari koje obično nisu svojstvene ovom tkivu. Na primjer, glikogen je u bubrezima, keratin je u suznoj žlijezdi.
Ovi patološki mehanizmi mogu se razviti uzastopno ili istovremeno. Morfološki, distrofije će se manifestirati kao kršenje strukture stanica. Obično, nakon oštećenja različitih ćelijskih struktura, počinje njihova regeneracija. U patologiji se krši čak i na molekularnom nivou. Unutar ćelija počinju se identificirati razna zrna, kapljice, kristali i druge inkluzije kojih ne bi trebalo biti, ili je njihov broj u zdravim stanicama neznatan. Proces se može odvijati i u suprotnom smjeru – u stanicama nestaju inkluzije ili dijelovi organela koji su im uobičajeni.
Na nivou organa, distrofija se manifestuje promjenom izgleda. Boja, veličina, oblik se mijenja, za takve procese se kaže da su "ponovno rođenje" ili degeneracija organa. Tijelo mijenja svoje funkcioniranje - sinteza raznih tvari, metabolizam. Ako se etiologija distrofije može ukloniti i nema dubokog oštećenja, postoji mogućnost apsolutne restauracije organa. U drugim slučajevima, procesi su nepovratni, razvija se nekroza.
Vrste distrofije
Klasificiraju se prema stepenu štete koju uzrokuju:
parenhimski - zahvaćaju parenhim organa; stromalno-vaskularni - preraspodjele u mikrožilama i međućelijskom prostoru; mješoviti.
Ako uzmemo u obzir patologiju određenog metabolizma:
proteini, masti, ugljeni hidrati, minerali.
Po obimu procesa su:
lokalni, opšti ili sistemski.
Postoje i stečeni i nasljedni.
Parenhimske disproteinoze
Promjena u metabolizmu citoplazmatskih proteina, koji su u vezanom ili slobodnom stanju, naziva se proteinska distrofija. Vezani proteini su različiti kompleksi lipoproteina, dok su slobodni proteini predstavljeni ćelijskim enzimima. Njihova fizička i hemijska struktura se menja, u citoplazmi se formiraju različite peptidne čestice. To podrazumijeva promjenu izmjene vode i elektrolita, osmotski tlak i povećanje zasićenosti tekućinom.
Morfološki se to manifestuje hijalin-kapljičnom i hidropičnom distrofijom. Završna faza njihovog postojanja može biti nekroza ćelija. Završna faza metaboličkog poremećaja hijalinske kapi je koagulativna nekroza, sa hidropičnom na kraju nekroze kolikvatne ćelije. Ove promjene moguće je razmotriti samo uz korištenje mikroskopije oštećenih područja. Kod disproteinoze hijalinskih kapi, hijalinske kapi se skupljaju u ćelijama. Ćelije zahvaćene hidropičnom distrofijom povećavaju volumen zbog vakuola s tekućim providnim sadržajem.
Zrnasta distrofija, ili mutno oticanje - takođe parenhimska distrofija, gubitak proteina u obliku zrna. Uzroci su razne infekcije, patologija cirkulacije, pothranjenost. Funkcionalno, ne narušava funkcionisanje organa i ponekad se povlači bez traga.
Hidropična distrofija, naprotiv, uzrokuje depresiju funkcije jetre. Razvija se u pozadini teškog i umjerenog virusnog hepatitisa, produžene kolestaze, distrofičnog oblika ciroze. Najizraženiji tip je balon distrofija, koja s produženim porastom postaje ireverzibilna i prelazi u kolikvacijsku nekrozu. Ćelije se zatim tope u tečno stanje. U fokus dolaze imune ćelije koje uklanjaju mrtvo tkivo. Na njihovom mjestu se formira ožiljak.
Hijalinska kap distrofija u jetri se manifestira smanjenjem veličine ćelija, zadebljanjem proteinskih formacija. Posebna vrsta su alkoholna hijalina ili Malloryjeva tijela. Ovo je poseban protein, rezultat sinteze hepatocita. Nalazi se u ćelijama oko jezgra i ima acidofilnu reakciju (obojena plavo). Ima leukotaksiju - privlači leukocite, može izazvati imunološke reakcije, stimulira stvaranje kolagena. U krvi oboljelih od alkoholizma nalaze se cirkulirajući imuni kompleksi na bazi alkoholnog hijalina, koji mogu utjecati na bubrege uz nastanak glomerulonefritisa.
Parenhimska lipidoza
Masna degeneracija je stvaranje velike količine lipida u stanicama ili taloženje u područjima gdje ih ranije nije bilo, kao i sinteza masti nekarakteristične strukture.
Najveći dio akumuliranih masti u hepatocitima je neutralna mast. Formira kapljice koje se postepeno spajaju u veliku vakuolu. Metabolizam masti je poremećen u tri slučaja:
Ogroman unos masti u organizam, što na kraju dovodi do nedostatka enzima za njihovu probavu.Otrovne supstance blokiraju sintezu masti.Nedostatak aminokiselina za stvaranje lipoproteina i fosfolipida.
Sljedeći faktori izazivaju razvoj lipidoza:
alkoholizam; dijabetes melitus; opća gojaznost; toksična oštećenja; nasljedna fermentopatija; bolesti probavnog sistema.
Masna jetra se manifestuje u tri oblika:
diseminirano - lipidne kapljice se nalaze u odvojenim ćelijama; zonsko - masti se skupljaju u posebnim područjima jetrenog lobula; difuzno - distribucija masti po cijelom lobulu.
Prema veličini inkluzija, gojaznost može biti velika i mala.
Dugotrajna konzumacija alkohola u skoro 50% završava se formiranjem masne hepatoze
Etilni alkohol i njegovi metabolički produkti povećavaju sintezu masnih kiselina, ali smanjuju njihovu oksidaciju i stvaranje lipoproteina. Kolesterol se nakuplja u velikim količinama, što smanjuje propusnost ćelijskih membrana. Intracelularne kapljice masti guraju jezgro na periferiju. Ali sintetički rad ćelije nije prekinut. Odbijanjem alkohola dolazi do obrnutog razvoja procesa. Funkcije se obnavljaju, akumulirani lipidi se postupno metaboliziraju i izlučuju iz jetre.
Ali ako pacijent više voli piti alkohol, tada to prijeti prijelazom masne degeneracije u cirozu.
Kod pacijenata sa dijabetesom, masna degeneracija se razvija u 70% slučajeva. Na to utiču takvi faktori:
dob - češće kod starijih osoba; dijabetes tipa 2 povezan je s pretilošću ili poremećenim metabolizmom lipida; ozbiljnost ketoacidoze.
Kao rezultat nedostatka inzulina i ulaska glukoze u stanice, aktivira se lipoliza - metabolizam masti, usmjeren na zadovoljavanje energetske gladi. Koncentracija masnih kiselina u krvi raste, jetra ih pokušava preraditi u lipoproteine. Višak ide na resintezu triglicerida. Ali previše se zadržava u hepatocitima, uzrokujući masnu hepatozu.
Masna degeneracija jetre je reverzibilan proces. Tu glavnu ulogu igra prestanak utjecaja provocirajućeg faktora - isključenje alkohola, normalizacija sastava hrane, smanjenje količine masti, kontrolirani tok dijabetesa.
Masna degeneracija trudnica
Odvojeno, vrijedi razmotriti razvoj akutne masne hepatoze tijekom trudnoće. Ovo je ozbiljno stanje koje često uzrokuje smrt majke ili fetusa. Uzroci nastanka nisu u potpunosti poznati. Pretpostavimo utjecaj naslijeđa, genetski determinisan defekt u mitohondrijskom enzimskom sistemu. To uzrokuje poremećaj oksidacije masnih kiselina.
Simptomi patologije su različiti. Neki možda neće razviti žuticu. Ali češće postoji klasični tok: slabost, letargija, mučnina, žgaravica. Žutica se postepeno povećava, njena značajna težina predstavlja opasnost za majku i fetus. Na pozadini žgaravice nastaju čirevi na jednjaku, moguće je povraćanje "taloga od kafe" uz nastalo krvarenje iz jednjaka. Zatajenje jetre se razvija sa slikom zamagljenja svijesti. Često je to praćeno sindromom diseminirane intravaskularne koagulacije, što uzrokuje smrt.
Sumnja na razvoj akutne masne hepatoze u 3. tromjesečju trudnoće indikacija je za hitan porođaj radi spašavanja života majke i djeteta.
degeneracija ugljenih hidrata
Očituje se kršenjem strukture ili taloženjem oblika ugljikohidrata na atipičnim mjestima. Često je to oblik skladištenja - glikogen. Kod dijabetesa i glikogenoze takvi procesi postaju mogući.
Kod dijabetičara je sadržaj glikogena u stanicama značajno smanjen, ali se nakuplja u jezgrama, zbog čega dobivaju „prazan“ izgled, otklanjaju se duž krvnih žila i živaca, što ih oštećuje i dovodi do razvoja dijabetičke angiopatije. .
Ako se količina glikogena u tkivima poveća, ovo stanje se naziva glikogenoza. To se opaža kod anemije, leukemije, na mjestima upale. Akumulira se u mišićima, srcu, bubrezima, vaskularnim zidovima. Klinički se može manifestirati kao srčana ili respiratorna insuficijencija sa smrtnim ishodom.
Simptomi
Osnovna bolest koja je izazvala distrofiju će dati simptome. Akutne procese prati slabost, malaksalost, smanjena učinkovitost. Istezanje kapsule jetre ili bolest žučne kese će biti praćena bolom. Često je tup bol ispod rebara sa desne strane. Ponekad zrači u leđa, u područje desnog bubrega, u vrat, lopaticu, rame s desne strane.
Pacijenti su zabrinuti zbog dispeptičkih simptoma - mučnina, žgaravica, može biti povraćanje. Stolica je slomljena, javljaju se periodi zatvora i dijareje, često praćeni nadimanjem, nadimanjem.
Nakon nekoliko sati ili dana može se pojaviti simptom žutice, kao manifestacija poremećaja metabolizma bilirubina. Prvi koji reaguju su izmet i urin. Izmet postaje bezbojan, a urin postaje boje piva. Istovremeno, uznemiruje i pruritus - iritacija kožnih receptora cirkulišućim žučnim kiselinama.
Kod uznapredovalih distrofičnih procesa postoje znakovi kršenja metabolizma proteina. Smanjen je imunitet, češće se javljaju zarazne bolesti. Nedostatak sinteze proteinskih faktora koagulacije manifestuje se krvarenjem desni, krvarenjima u koži, hemoroidnim, gastrointestinalnim, krvarenjem iz materice.
Nedostatak proteina dovodi do nedovoljnog vezivanja vode, što se manifestuje višestrukim edemom, razvojem ascitesa.
Ekstremni stepen zatajenja jetre je hepatična encefalopatija. Ovo je sindrom koji nastaje kao posljedica metaboličkog poremećaja, a manifestira se promjenom svijesti, ponašanja i neuromišićnih reakcija. Može se razviti akutno u roku od 7 dana ili duže, tokom 3 mjeseca.
Ozbiljnost kršenja ovisi o brzini razvoja i uzrocima koji su uzrokovali ovo stanje. Postoje poremećaji ličnosti, oštećenje pamćenja i smanjena inteligencija.
Encefalopatija se javlja u tri faze:
Lagane promjene ličnosti, pritužbe na poremećaj sna, smanjenu pažnju i pamćenje. Teški poremećaji ličnosti, često neprimjereno ponašanje, promjene raspoloženja, pospanost, monoton govor. Vremenska dezorijentacija, stupor, promjene raspoloženja, agresivnost, deluzija, patološki refleksi. Hepatična koma - duboka depresija svijesti, smanjenje tetivnih refleksa, pojava patoloških.
Osim neuroloških znakova, postoje i drugi klinički simptomi - žutica, smrad na jetri, groznica, tahikardija. Uz opsežnu nekrozu, infekcija se može pridružiti. Smrt često nastupa od cerebralnog edema, zatajenja bubrega, plućnog edema, toksičnog ili hipovolemijskog šoka.
Dijagnostika
Pregled počinje prikupljanjem podataka iz anamneze:
pritužbe pacijenata; vrijeme pojave znakova bolesti; njihov razvoj tokom vremena; povezanost sa različitim faktorima - konzumacija alkohola, ishrana, fizička aktivnost; indikacija nezaštićenih seksualnih kontakata, injekcija, posjeta stomatologu, tetovaža, transfuzije krvi u posljednjem 6 mjeseci; prisutnost gastrointestinalnih oboljenja crijevnog trakta, jetre, dijabetesa, trudnoće.
Opšti pregled otkriva višak kilograma, promjenu boje kože, grebanje, krvarenje po koži, osip, pigmentaciju, oticanje ekstremiteta ili nakupljanje tekućine u trbušnoj šupljini.
Distrofija jetre je morfološka karakteristika procesa koji su uzrokovani utjecajem različitih patogenih faktora. Dakle, dijagnoza ima za cilj da se ustanovi bolest koja je dovela do razvoja distrofije organa. Za to se koriste laboratorijske dijagnostičke metode. Kompletna krvna slika pokazuje prisustvo upale u organizmu. Biohemijski test krvi omogućava procjenu stanja sintetičke funkcije jetre, prisutnosti citolitičkih reakcija i oštećenja stanica.
U toku je istraživanje markera virusnog hepatitisa, koji takođe uzrokuje distrofiju jetre.
Sljedeći korak je ultrazvuk. Metoda je neinvazivna i omogućava otkrivanje difuznih ili žarišnih promjena u tkivu. Po prirodi ultrazvučne slike može se pretpostaviti masna infiltracija jetre, razvoj fibroze ili ciroze. Na ultrazvuku su jasno vidljive volumetrijske formacije, šupljine, ciste, kalcifikacije, uočljivi su znakovi portalne hipertenzije.
Korištenje rendgenskih metoda omogućuje vam da utvrdite prisutnost promjena u jetri, povećanje njene veličine. Kontrastiranje žučnih puteva ili krvnih žila pokazuje njihovo stanje, zakrivljenost, prisustvo suženja, opstrukciju odljeva žuči. Koriste se i metode kao što su CT i MRI. Nema specifičnih znakova koji ukazuju na razvoj distrofije. To se može pretpostaviti otkrivanjem promjena u parenhima karakterističnih za različite bolesti.
Morfološka slika se može utvrditi samo uz pomoć biopsije. Ali ovo je traumatična metoda koja može dovesti do ozbiljnih komplikacija. Stoga se koristi samo prema indikacijama:
pojašnjenje etiologije oboljenja jetre; hronični virusni hepatitis; bolesti skladištenja (hemohromatoza, Wilsonov sindrom); bilijarna ciroza za određivanje stepena upalnog odgovora i fibroznih promena; karcinom; praćenje efekta lečenja ovih bolesti.
Postoje stanja u kojima je ova metoda apsolutno kontraindicirana:
ozbiljno stanje pacijenta; menstrualno krvarenje kod žena; znaci kršenja zgrušavanja krvi; smanjenje razine trombocita; opstruktivna žutica.
Za dijagnozu masne degeneracije nije preporučljivo koristiti metodu. Ovaj oblik ima sposobnost regresije pod utjecajem liječenja i dijete. Stoga će podaci dobijeni iz studije biti irelevantni nakon 2-3 sedmice.
Tretman
Da biste se efikasno nosili sa bolešću, terapija treba da prođe kroz sledeće korake:
racionalna prehrana; liječenje prateće patologije; obnova jetre; konsolidacija rezultata.
Konzervativna terapija
Liječenje popratnih bolesti sastoji se u adekvatnoj terapiji dijabetes melitusa koju propisuje endokrinolog. Bolesti gastrointestinalnog trakta liječe gastroenterolog ili lokalni internista. Za liječenje ovisnosti o alkoholu, ako osoba nije u stanju da se izbori sa željom za alkoholom, uključuje se narkolog.
Za liječenje se koriste lijekovi različitih grupa:
Hepatoprotektori, antioksidansi, statini.
Hepatoprotektori mogu imati različite efekte. Stabiliziraju ćelijske membrane, vraćaju njihov integritet i poboljšavaju sintetičke sposobnosti ćelija. Doprinose poboljšanju metabolizma bilirubina, masnih kiselina, proteina. Predstavnici grupe su lijekovi Karsil, Liv-52, Hofitol, Essentiale, ursodeoksiholna kiselina i lijekovi na njenoj osnovi.
Koriste se i koleretici Allohol, Holsas. Poboljšavaju sintezu žuči, njeno lučenje, regulišu sastav, smanjuju zastoje u jetri.
Statini se koriste za korekciju lipidnog profila krvi. Smanjuju apsorpciju masti u crijevima, uklanjaju višak kolesterola, sprječavajući ga da se vrati u krv.
Liječenje teškog oblika distrofije, praćene hepatičnom encefalopatijom, odvija se u jedinici intenzivne njege. Liječenje je simptomatsko. Pacijent se prebacuje na parenteralnu ishranu i davanje tečnosti, količina proteina je ograničena. Za korekciju kiselo-baznog stanja koriste se lijekovi, često se kod ovog stanja razvija acidoza, pa je neophodno uvođenje natrijum bikarbonata. Antibiotici se propisuju za suzbijanje crijevne flore.
Ponekad postoji potreba za ekstrakorporalnom detoksikacijom, posebno nakon dodavanja zatajenja bubrega. Za održavanje ukupnog metabolizma u velikim dozama koriste se glukokortikoidi. Ovo stanje se često završava smrću.
Liječenje narodnim metodama
Biljna i tradicionalna medicina mogu se koristiti kao pomoćne metode liječenja nakon konsultacije sa ljekarom. Nude razne recepte za rješavanje distrofije.
Dnevno možete konzumirati 2 supene kašike limunovog soka pomešanog sa istom količinom vode.
U roku od mesec dana popijte 2 čaše dnevno infuzije od plodova čička, korena maslačka, koprive, listova breze. Ova mješavina se prelije čašom kipuće vode i infundira 15 minuta.
Ako zreloj bundevi odrežete vrh i uklonite sjemenke, dobijete posudu u koju treba uliti svježi med i staviti na tamno i hladno mjesto na pola mjeseca. Nakon toga, dobiveni terapeutski sastav sipajte u staklenku i konzumirajte jednu žlicu prije jela.
Na prazan želudac mjesec dana piju mješavinu svježe iscijeđenog soka od šargarepe i toplog mlijeka u jednakim omjerima.
Sjemenke čička sameljite u prah. 3 supene kašike zakuhati 0,5 litara vode, prokuvati do pola. Pijte po supenu kašiku sat vremena pre jela 1 mesec.
Učinkovito pomaže odvar od sušenih krušaka i zobenih pahuljica. Uzmite 4 kašike ovsene kaše za čašu voća, prokuvajte u litru vode. Pojedite cijelu porciju tokom dana.
Gospina trava, preslica, šipak, izdanci matice pomiješani u jednakim dijelovima. Prokuvajte kašiku mešavine u čaši vode. Dobijenu čorbu popijte tokom dana, podeljenu u 4 doze.
Pomiješajte supenu kašiku latica cvetova divlje ruže sa pola kašike meda. Ovu mešavinu jedite posle jela sa čajem.
Dijeta
Liječenje jetre ne podrazumijeva strogu dijetu za gubitak težine. Glad će učiniti još veću štetu. Ishrana treba da bude uravnotežena u lipidno-proteinskom sastavu. Sadržaj masti je ograničen zbog životinjskog porijekla - puter, sirevi, mast, meso masnih rasa. To će smanjiti zasićenost hrane mastima, smanjiti njihovu apsorpciju, a samim tim i negativan utjecaj na jetru.
Količina proteina, naprotiv, treba povećati na račun životinjskih proizvoda. Upravo njihovi proteini imaju kompletan sastav aminokiselina, sadrže nezamjenjivu grupu. Proteini su potrebni za sintetičke procese jetre - izgradnju vlastitih enzima, stvaranje lipoproteina iz masti, proizvodnju raznih proteina ljudskog tijela - imunološki sistem, zgrušavanje krvi.
Količina ugljikohidrata je najveća, oni su energetski supstrat. Ali moramo imati na umu da se prednost daje biljnim ugljikohidratima, vlaknima, dijetalnim vlaknima. Jednostavni šećeri sadržani u slatkišima, bogatim pecivima, brzo se obrađuju, značajno podižu nivo glukoze, što će zakomplicirati situaciju pacijenta.
Alkohol je apsolutno zabranjen, on je jedan od razloga za nastanak distrofije, pa ga u prvom redu treba isključiti.
Dijeta se može opisati kao mliječno-vegetarijanska dijeta sa dodatkom nemasnog mesa i ribe. Povrće i voće se mogu konzumirati u bilo kom obliku. Izuzetak su kiseljak, mahunarke, gljive.
Količina soli se smanjuje na 15 g dnevno. Da ne bi pogrešili, hrana se kuva bez soli, soljena na tanjiru.
Ako je uzrok distrofije dijabetes melitus, ishranu treba graditi na sistemu hljebnih jedinica. Izračunava količinu ugljikohidrata koja je potrebna za osobu dnevno. Raspodijele se prema obrocima, a zatim prema posebnim tablicama određuju koliko se jednog ili drugog proizvoda može pojesti. Ovaj sistem pomaže u kontroli nivoa glukoze kod dijabetičara, smanjuje težinu. Može se koristiti i za ishranu osoba sa prekomjernom težinom. Višak težine će postepeno nestati.
Ako je distrofija jetre dostigla teško stanje jetrene encefalopatije, tada se prehrana drugačije gradi. Količina proteina je ograničena na 50 g dnevno. To je neophodno kako bi se jetra mogla nositi s detoksikacijom proizvoda metabolizma proteina. Ako se stanje pogorša, generalno se ukida, započinje parenteralna prehrana.
Prevencija i prognoza
Prevencija je usmjerena na uklanjanje faktora rizika za stanja i bolesti koje dovode do razvoja distrofičnih procesa. Višak kilograma se mora držati pod kontrolom, pokušajte ga svesti na prihvatljive brojke. Da biste to učinili, prvo morate odrediti indeks tjelesne mase. Ako je iznad 25, onda je vrijeme da razmislite o gubitku težine.
Čak i ako je težina normalna, ali u ishrani dominiraju namirnice bogate mastima, trebali biste pokušati smanjiti njihovu količinu, to će smanjiti opterećenje na enzimskim sustavima jetre.
Gladovanje i krute dijete neće donijeti koristi. Nedostatak proteina će uzrokovati pothranjenost i razvoj masne degeneracije, jer. neće biti supstrata za sintezu molekula proteina i masti.
Alkohol, čak i uz malu, ali redovitu upotrebu, toksično djeluje na stanice jetre, oštećuje ih i uzrokuje patološke mehanizme za sintezu netipičnih hijalinskih proteina ili taloženja masti. Potpuno odbijanje alkohola u ranim fazama masne degeneracije može dovesti do poboljšanja stanja pacijenta. S uznapredovalom cirozom, to će spriječiti nastanak hepatične encefalopatije i terminalnu fazu.
Virusno oštećenje jetre može se izbjeći ako se zna o putevima prijenosa. Da biste spriječili hepatitis A, morate se pridržavati lične higijene, prati ruke, voće i ne koristiti vodu za piće iz otvorenih izvora. Virusi tipova B i C se prenose krvlju, stoga pri izvođenju invazivnih zahvata koristite jednokratne instrumente, koristite samo lični komplet za manikir, nemojte imati nezaštićeni seksualni odnos, a nakon transfuzije krvi, nakon 6 mjeseci se pregledajte na hepatitis.
Žene tokom planiranja trudnoće treba da minimiziraju manifestacije postojećih hroničnih bolesti gastrointestinalnog trakta, patologije bilijarnog trakta. U trudnoći, kao rezultat hormonalnih promjena, postoji rizik od razvoja gestacijskog dijabetesa melitusa, koji se može manifestirati masnom hepatozom kao latentnim nasljednim poremećajem metabolizma estrogena. Stoga, pridržavanje dijete s malo masti i jednostavnih ugljikohidrata spriječit će disfunkciju jetre.
Sve bolesti gastrointestinalnog trakta treba pravovremeno dijagnosticirati i liječiti.
Masna degeneracija jetre naziva se i lipoidoza, hepatoza, steatoza, steatohepatoza. To je hronična, neupalna bolest.
Glavne promjene koje se dešavaju u organizmu su nakupljanje masnog tkiva koje kasnije formira kapsule – ciste. S vremenom, ako se ne liječe, mogu puknuti i uzrokovati ozbiljnije komplikacije. Glavni razlog je poremećen metabolizam, koji može biti izazvan raznim faktorima.
Najčešće se patologija razvija nakon 46-50 godina.
Poremećen metabolizam dovodi do toga da jetra ne može lučiti pravu količinu enzima za obradu masti.
Kao rezultat toga, počinju se akumulirati u šupljini organa.
Takve promjene mogu nastati pod utjecajem sljedećih faktora:
- Poremećaj ishrane. Slatkiši, gotova i brza hrana, konzervansi, boje i drugi toksini su posebno štetni za jetru.
- Produženi post ili, obrnuto, stalno prejedanje. Dijeta izgladnjivanja ili pogrešno sastavljena ishrana, vegetarijanstvo su neprijatelji jetre. Oni dovode do telesne masti.
- nasledni faktor. Ako je u porodici bilo rođaka sa bolestima jetre, tada će osoba razviti distrofičnu patologiju u 89%.
- Nekontrolisana i produžena upotreba lekova.
- Konzumiranje previše alkohola (alkoholna masna bolest jetre).
- Upotreba droga.
- Profesionalna djelatnost koja uključuje rad u industrijskim preduzećima gdje se proizvode različite vrste hemikalija.
- Pasivni stil života.
- Poremećaj hormonskog sistema.
- Neoplazme koje utječu na hipofizu.
Mehanizam nastanka masne degeneracije je zapravo vrlo jednostavan. Masti ulaze u gastrointestinalni trakt (gastrointestinalni trakt) i podložne su procesu cijepanja. Ako mnogo ovih komponenti ulazi u jetru, a postoje faktori odlaganja, masti se podvrgavaju sintezi i akumuliraju u ćelijama jetre. Ista stvar se događa pod djelovanjem tvari koje sadrže ugljikohidrate i koje ulaze u jetru u velikim količinama.
Masna degeneracija se može klasificirati na sljedeći način:
Tip I - masne inkluzije su jednostruke prirode, nasumično se nalaze u jetri. Nema kliničkih manifestacija.
Tip II - molekuli masti su gusto zbijeni. Osoba se osjeća lošije, ima bolova u jetri.
Tip III - postoji lokalni raspored masnih kapsula, nalaze se u određenim dijelovima tijela. Simptomi su izraženi.
Tip IV - masne molekule nalaze se gotovo u cijeloj jetri ili zauzimaju jedan od režnja. Simptomi su jasni.
Masna degeneracija se također može klasificirati ovisno o stadiju:
I - ćelije jetre sadrže malu količinu masnih molekula, ali one ne utječu na funkcioniranje organa, iako je destruktivni mehanizam već pokrenut.
II - mast u potpunosti ispunjava ćelije, one se uništavaju, oko svake ćelije se može razviti upalni proces.
III - procesi su nepovratni, razvija se nekroza, u većini slučajeva je nemoguće vratiti funkciju jetre u ovoj fazi.
Kako se bolest manifestuje
Simptomi masne degeneracije direktno zavise od stadijuma bolesti, koliko je jetra zahvaćena. Prvi stadij karakterizira asimptomatski tok bolesti.
Simptomi bolesti pojavljuju se već u drugoj fazi:
- Crtež, bolan bol u predelu jetre, koji se pogoršava nakon konzumiranja masne hrane, dimljenog mesa, začinjenih jela i alkoholnih pića. Bol može biti stalna ili povremena.
- Gorčina u ustima, podrigivanje sa gorkim ukusom.
- Mučnina, koja se gotovo uvijek završava povraćanjem.
- Nadutost.
- Povećanje jetre u veličini.
- Na jeziku se pojavljuje žuta prevlaka, gusta je.
- Zatvor praćen proljevom. Oni su trajni.

Znakovi treće faze lezije uzrokuju vrlo veliku nelagodu i izražavaju se u:
- povećana razdražljivost;
- poremećaj spavanja;
- umor;
- oštećenje pamćenja;
- sklonost ka depresiji;
- nakupljanje velike količine (do 25 l) slobodne tekućine (trbuh postaje vrlo velik);
- bol se ne može ublažiti analgeticima;
- žutilo kože;
- u rijetkim slučajevima razvija se svrab.
Ako masna degeneracija dovede do nekroze tkiva jetre, uočavaju se sljedeći dodatni znakovi i simptomi:
- neprijatan miris jetre na krevetu i iz usne duplje;
- značajno povećanje temperature;
- krvarenje iz nosa;
- anoreksija;
- srčane aritmije i nedostatak daha.

Treba napomenuti da čim se pojave prvi simptomi, trebate odmah otići u bolnicu kako bi liječnik propisao tijek liječenja. Ni u kom slučaju ne možete sami liječiti masnu degeneraciju. Ovo može dovesti do smrti. Druga stvar je da se bolest razvija prilično brzo, pa liječenje treba propisati što je prije moguće.
Danas, uz blagovremeni prijem u bolnicu, liječenje je efikasno, zahvaljujući inovativnim metodama i lijekovima nove generacije.
Nije zabranjeno koristiti narodne metode liječenja, ali je potrebno konzultirati liječnika prije pijenja dekocija.
Alkoholne tinkture su zabranjene. Masna degeneracija ne podnosi alkohol.
Kako se provode dijagnostičko testiranje i liječenje?
Dijagnostika uključuje sljedeće vrste pregleda:

- ultrazvučni postupak;
- CT skener;
- laparoskopska tehnika;
- biopsija za identifikaciju masnih inkluzija, njihovog broja, veličine i lokalizacije;
- krvne pretrage.
Kada se prouče simptomi, kao i na osnovu dijagnostičkog pregleda, propisuje se liječenje, čija će se shema razvijati u svakom pojedinačnom slučaju.
Liječenje masne degeneracije provodi se u kompleksu. U ovom slučaju, preduslov je dijeta.
Samo poštujući sve recepte liječnika, bit će moguće riješiti se masne degeneracije. Za liječenje distrofije, liječnici propisuju lijekove za obnavljanje stanica jetre, lijekove koji normaliziraju metabolizam, lijekove i vitaminski kompleks za jačanje imuniteta. Ako je prisutan upalni lijek, liječenje uključuje uzimanje protuupalnih lijekova.
Liječenje narodnim lijekovima
Liječenje distrofije jetre može se provesti bundevom.

Veoma je bogat vitaminima i mineralima koji pomažu u najkraćem mogućem roku da se obnove ćelije i normalizuje metabolička ravnoteža.
Odrežite vrh bundeve, uklonite sjemenke, napunite šupljinu medom i stavite na hladno mjesto 8-10 dana. Nakon toga, ocijedite med u posudu i stavite u hladnjak. Uzmite 1 tbsp. l. 2 puta dnevno. Ako ste alergični na pčelinje proizvode, ova metoda je zabranjena.
Moguće je liječiti distrofiju biljnom kolekcijom. Sljedeće komponente se uzimaju u jednakim količinama: struna, pelin, žalfija, listovi maline, breza, kamilica, stolisnik, lipa. Sameljite i pomiješajte sastojke. Ulijte kipuću vodu u omjeru 1 dio kolekcije, 2 dijela vode. Dajte 3 sata, procijedite i uzimajte u toku dana kao čaj.
Možete liječiti distrofiju uz pomoć takvog izvarka: listova breze, divlje ruže, gloga, planinskog pepela s crvenim plodovima, listova koprive, brusnice, medvjeđe bobice, korijena maslačka, plodova komorača, gospine trave. Sameljite komponente i sipajte vodu u omjeru 1:3. Smesu kuvajte na parnom kupatilu 20 minuta. Procijedite i pijte kao čaj tokom dana.
Bitan! Narodni recepti ne mogu biti glavni tretman! Samo u kombinaciji sa terapijom lijekovima dat će rezultate.
Dijeta za distrofiju jetre
Osnovna pravila dijete:

- povećati količinu hrane bogate proteinima (kiselo-mliječni proizvodi, nemasno meso);
- isključiti ugljene hidrate (beli hleb, šećer, pirinač, krompir);
- smanjite količinu životinjskih masti (maslac, masna riba i puter);
- obavezno uključite u prehranu najmanje 2,5 litara vode dnevno;
- isključiti alkohol;
- odbijte prženu, začinjenu, slanu hranu.
Kako će se distrofija liječiti zavisi od osobe. Ako postoji višak kilograma, osoba vodi sjedilački način života, trebali biste se potpuno riješiti takvih faktora - baviti se sportom, ali bez puno fizičkog napora. Možete pitati svog doktora o tome kako liječiti distrofiju fizičkom gimnastikom.
Glavni zadaci dijetetske prehrane kod distrofije su normalizacija glavnih funkcija organa i nastavak metabolizma kolesterola i masti; stimulacija proizvodnje žuči.
Količina masti koja se konzumira tokom dana ne bi trebalo da prelazi 50 g! Ovo je veoma važan uslov.
Osim toga, potrebno je isključiti hranu koja je bogata holesterolom. U ovom slučaju, bit će moguće ne samo pomoći stanicama jetre da se oporave, već i izbjeći tromboflebitis.

Još jedno važno pravilo je da jela najbolje kuhati na pari ili jesti kuhana, pečena. U ovom slučaju neće biti korisni samo za jetru, već će i zadržati sve vitamine.
Šta treba uključiti u ishranu:
- juhe na juhi od povrća sa žitaricama, boršč;
- povrće;
- salate od povrća;
- blagi sir, šunka;
- kuhano jaje ili parni omlet;
- zobene pahuljice, heljda, griz;
- mlečni proizvodi sa niskim sadržajem masti.
Šta isključiti:
- masna hrana, juhe od gljiva i gljive;
- morski plodovi;
- svježi luk, bijeli luk, paradajz, rotkvice, mahunarke;

U kontaktu sa
Drugovi iz razreda
Normalan život bez masti je nemoguć. Nakon unosa hranom, razgradnjom u crijevima, masne kiseline se apsorbiraju u krv kroz zid gastrointestinalnog trakta i ulaze u jetru na dalju obradu.
Rezultat fiziološkog restrukturiranja je stvaranje holesterola, fosfolipida neophodnih za izgradnju ćelijskih membrana, stvaranje hormona, učešće u biohemijskim reakcijama.
Opisujući šta su simptomi i liječenje masne jetre, koji imaju specifičnost, uočavamo kršenje procesa prirodnog iskorištavanja lipida od strane hepatocita sa visokom akumulacijom masti (preko 50%). Citoplazma, vakuole i neke druge intracelularne organele su zasićene mastima, pa ne mogu obavljati svoje funkcije. Fiziološki, koncentracija masnih kiselina unutar ćelija jetre ne prelazi 5%. Kod masne degeneracije, u zavisnosti od stepena, ovaj nivo je prekoračen. Stanje je nepovratno, jer nedostatak pretvaranja lipida u energiju ili taloženje viška u potkožnom masnom tkivu dovodi do odumiranja i degeneracije jetrenog parenhima. Morfološki, sa ovom nozologijom, unutar lizozoma se pojavljuju mali klasteri (forma malih kapljica) ili veliki depoziti (varijetet velikih kapljica).
Etiološki i patogenetski mehanizmi bolesti nisu utvrđeni, pa se ne može u potpunosti izliječiti. Naučnici su identifikovali provocirajuće faktore koji dovode do degeneracije lipida:
- Zloupotreba alkohola kod muškaraca remeti procese unutarćelijskog metabolizma masti. Blokiranje biohemijskih reakcija dovodi do poteškoća u fiziološkoj upotrebi jedinjenja, a višak holesterola se akumulira u lizosomima;
- Mehanizmi biohemijske transformacije lipida također su narušeni kod dijabetes melitusa. Uzrok stanja je nedostatak glukoze neophodne za metaboličke reakcije;
- Gojaznost dovodi do viška naslaga u lipidnom depou potkožnog masnog tkiva. Prekomjerna akumulacija dovodi do nedostatka puteva izlučivanja, pa dolazi do intracelularne infiltracije;
- Metaboličke bolesti (nedostatak proteina) remete transportne procese između jetre i drugih tkiva;
- Trovanje hepatotoksičnim otrovima, lijekovima.
Opisani provocirajući mehanizmi rezultat su praktičnih zapažanja, ali patogenetske veze nozologije nisu dokazane naučnim istraživanjima. Potreba za ranim liječenjem je zbog razvoja ciroze, kada degeneracija dovodi do rasta grubih cirotičnih ožiljaka. Što je veća destrukcija, to je veći stepen zatajenja jetre.
Glavni simptomi masne degeneracije
Distrofični sindrom s intrahepatičnim viškom masnih inkluzija na pozadini upotrebe etilnog alkohola ima nekoliko sinonima "hepatosteatoza", "masna jetra", "steatohepatitis". Sorte odražavaju raznolikost patogenetskih mehanizama procesa. Dugotrajna upotreba etanola je praćena upalom, općim degenerativnim promjenama, blokadom metaboličkih reakcija.
Teški simptomi masne degeneracije, koji se klinički mogu pratiti, imaju različite morfološke manifestacije. Prilikom pregleda biopsijskog uzorka (komad tkiva) uočava se nekoliko morfoloških varijanti distrofičnih promjena.
Kod kroničnog virusnog i toksičnog hepatitisa, ne samo lipidi, već i proteini se prekomjerno akumuliraju u hepatocitima. Morfološki pregled otkriva hijalinsku i hidropičnu granularnost. Osnova njegovog izgleda je uništavanje proteinsko-lipidnog kompleksa, koji je dio organela.
Klinički simptomi ovog oblika nastaju zbog osnovne bolesti:
- Bol u desnom hipohondrijumu;
- Pojava linearnog širenja krvnih žila u abdomenu;
- Kapilarne zvjezdice (telangiektazije) po cijelom tijelu.
Zrnaste distrofične promjene pojavljuju se na pozadini oksidativne fosforilacije, neravnoteže metabolizma vode i soli. Stanje je adaptivno, kompenzatorno usmjereno na obnavljanje intracelularnih poremećaja koji nastaju pod utjecajem virusa, bakterija i primjene hepatotoksičnih lijekova.
Klasičan znak parenhimske masne degeneracije na histohemijskom pregledu je jedna velika vakuola ispunjena masnim inkluzijama, gurajući jezgro ka periferiji.
Morfološkim pregledom uočava se žućkasto, mutno tkivo. Sa degeneracijom 50% ćelija, male vakuole ovalnog oblika mogu se pratiti u nekim hepatocitima. Postepeno se klasteri spajaju, a ćelije umiru. Formiranje masnih "cista" dovodi do stvaranja sljedećih morfoloških stanja:
- Segmentne naslage lipida za gojaznost su lokalizovane duž perifernih, centralnih delova lobula;
- Kapljice masti diseminirane hepatoze nalaze se u odvojenim ćelijama jetre;
- Difuznu pretilost karakterizira poraz cijelog lobula, ali je proces reverzibilan.
Kod dijabetes melitusa, manifestacije hepatoze nisu specifične. Masna degeneracija nastaje zbog kršenja metabolizma glikogena. Nedostatak inzulina dovodi do značajnog smanjenja rezervi ove tvari. Kompenzatorni hepatociti se povećavaju u veličini zbog taloženja glikogena. U uzorcima biopsije tkiva uočavaju se prazna jezgra, povećava se broj vakuola.
Kod dijabetesa se razlikuje deset različitih tipova glikogenoze, među kojima masna degeneracija nije česta opcija, ali se može vidjeti kod pacijenata s gojaznošću. Histohemijski pregled ćelija pokazuje nakupljanje specifičnih eozinofilnih granula.
Opisane promjene uzrokuju simptome u zavisnosti od stepena zatajenja jetre. Odsustvo klinike u odumiranju malog broja stanica posljedica je visokih restorativnih funkcija jetrenog tkiva. Samo s velikim oštećenjem razvija se zatajenje jetre, što dovodi do simptoma:
- Žutilo kože i bjeloočnice zbog kršenja lučenja žuči;
- Encefalopatija u slučaju trovanja toksinima, amonijakom;
- Osip na koži, svrab, povećana koncentracija bilirubina;
- Sindrom boli ispod rebara desno, povećanje veličine jetre, ciroza.
Ekstremni stepen insuficijencije je hepatična koma, nakupljanje tečnosti unutar abdomena (ascites). Nedostatak detoksikacijske funkcije dovodi do popratnog povećanja slezene, razvoja zatajenja bubrega. Svaki simptom jetre je opasan po život ako je praćen nakupljanjem toksina u krvi.
Liječenje distrofičnih stanja jetre
Alkoholnu steatozu doktori smatraju opasnim stanjem koje vodi do smrti. Nozologija izaziva opasne komplikacije sa prosječnim stupnjem degeneracije (oko 35% tkiva).
Početni stadijumi bolesti se zaustavljaju imenovanjem lijekova i prestankom konzumiranja alkohola, teške karakterizira visoka smrtnost. Otprilike 5% ljudi umre u roku od mjesec dana kada im se dijagnostikuje ciroza.
Ne postoje specifični lijekovi, stoga se simptomatska terapija provodi esencijalnim fosfolipidima (Essentiale), holereticima (ursodeoksiholna kiselina), ademetioninom, silibininom. Racionalnost propisivanja drugih hepatoprotektora je niska.
Kod alkoholnog hepatitisa virusnog ili bakterijskog porijekla, efikasnost liječenja hepatoprotektivnim lijekovima je smanjena. Za smanjenje progresije koriste se steroidni protuupalni lijekovi. Najčešći predstavnik prednizolona.
Efikasnost glukokortikoida u masnoj degeneraciji nije dokazana, ali u praksi se terapeutski efekat uočava u prisustvu 3 faktora:
- Povećan portalni pritisak;
- Nedostatak akumulacije dušika u krvi;
- Nema krvarenja u želucu.
U praktičnoj literaturi postoje naznake potrebe za pravilnom ishranom, koja povećava preživljavanje pacijenata.
Principi liječenja lipidne degeneracije hepatocita
- Uklanjanje faktora rizika;
- Medicinsko otklanjanje komplikacija;
- Dugotrajna upotreba hepatoprotektora.
Glavni faktor rizika za nastanak bolesti je gojaznost. Naučne studije su pokazale da smanjenje tjelesne težine za 10% dovodi do smanjenja koncentracije enzima holestaze (AlAt, AsAt).
Evropski stručnjaci ukazuju na potrebu postepenog smanjenja tjelesne težine. Optimalna ravnoteža Sedmična eliminacija više od jednog i po kilograma povećava rizik od bolesti žučnog kamenca, pa je potrebno paziti na dijetu.
Karakteristike dijetalne hrane:
- Sadržaj kalorija u prehrani nije veći od 1200 kcal dnevno;
- Ograničenje u hrani zasićenih masnih kiselina;
- Ugljikohidrati nisu više od 100 grama dnevno, ali nutricionisti mogu smanjiti ovu stopu.
Svakodnevno vježbanje doprinosi boljoj apsorpciji masti, nakupljanju kisika unutar mišićnih vlakana, što povećava potrošnju triglicerida.
Kod dijabetesa, gojaznost je uzrokovana rezistencijom na inzulin. Faktor potiče pretvaranje viška ugljikohidrata u masti. Korekcija inzulinske tolerancije postiže se farmakološkim agensima tiazolidindionima, bigvanidima.
Uklanjanje povišenih triglicerida postiže se redovnom upotrebom lijekova koji sadrže nezasićene masne kiseline. Proizvodi ursodeoksiholne kiseline koriste se već deset godina i pokazali su visoku efikasnost. Mehanizmi terapijskog djelovanja nisu dokazani, ali je otkrivena eliminirajuća aktivnost lijeka na eliminaciju kongestivnih promjena u žučnoj kesi i intrahepatičnim kanalima.
Kod teškog zatajenja jetre, sadržaj proteina u prehrani je ograničen. Dnevni sadržaj nije veći od 50 grama. Za čišćenje gastrointestinalnog trakta svakodnevno se propisuju laksativi i klistiri za čišćenje. Disbakterioza se otklanja uvođenjem antibiotika kroz sondu (ampicilin, kanamicin, tetraciklin).
Za neutralizaciju amonijaka arginin se daje u dozi od 50-75 grama dnevno.
Psihomotornu agitaciju zaustavlja haloperidol.
Terapija steatohepatitisa narodnim lijekovima
Ljekar propisuje biljne dekocije. Samo stručnjak će moći ispravno odrediti vrstu terapije, kombinaciju i dozu svakog lijeka. Ako se patologija otkrije na vrijeme, koleretički preparati smilja, mliječnog čička, šipka pomažu u ranoj fazi.
Biljni preparati smanjuju aktivnost kroničnog procesa, ali samo uz određene nozologije. Terapeutski učinak biljnih odvara i infuzija, u usporedbi s lijekovima, javlja se kasnije, pa je kombinacija lijekova s biljkama racionalna. Uz nisku procesnu aktivnost, možete koristiti bundevu:
- Odaberite zrelo voće, odrežite gornji rub u krug. Uklonite središnji dio, a u nastalu šupljinu dodajte lagani med. Voće zatvorite i ostavite 2 sedmice na tamnom mjestu. Dobijeni rastvor ocedite u teglu. Za lečenje uzimajte 3 supene kašike napitka tri puta dnevno ujutru, popodne i uveče.
Drugi korisni narodni recept za uklanjanje hepatoze su orasi. Da biste ga pripremili, potrebno je nasjeckati orahe. Sipajte ih u teglu, dodajte med i alkohol u jednakim razmerama. Infuzirajte lijek 1 mjesec u mračnoj prostoriji. Koristite tri puta dnevno po kašičicu.
Mliječni čičak je dio popularnih hepatoprotektora Karsil, Silibinin. Biljku možete koristiti kod kuće. Recept se priprema mešanjem maslačka, koprive, listova breze i mlečnog čička. 2 kašičice smjese preliti kipućom vodom, ostaviti 15 minuta. Uzmite 2 čaše lijeka dnevno.
Biljne infuzije i dekocije, u poređenju s tabletama, imaju blagi, postupni učinak. Da biste povećali efikasnost, preporučuje se kombiniranje narodnih lijekova s dijetom, vježbanjem.
Značajke prehrane za distrofična oštećenja hepatocita:
- Izbjegavajte začinjenu, začinjenu hranu;
- Odustanite od masnog mesa, ribe, čorbe;
- Pažljivo birajte svoje proizvode u trgovini. Ne smiju sadržavati boje, stabilizatore, mirise, aditive protiv zgrušavanja;
- Nemojte uzimati previše lijekova bez potrebe;
- Korisne zobene pahuljice, heljda.
Evropski naučnici ukazuju na efekat koštica kajsije topiv u mastima. Za steatohepatitis, jedite 5 komada dnevno (ali ne više). Centralni sadržaj voća je zasićen vitaminom B15, koji učestvuje u razgradnji lipida.
Šta je zapravo distrofija jetre?
Distrofija jetre, steatoza, lipodistrofija ili hepatoza - svi ovi pojmovi se odnose na istu kroničnu bolest u kojoj se ćelije jetre postepeno zamjenjuju masnoćom.
Treba napomenuti da je ova masna jetra prilično poznata, jer mnogi uobičajeni faktori mogu potaknuti razvoj ove bolesti. Hepatoza jetre - ovo je početna faza razvoja najpopularnije bolesti u modernom svijetu - ciroze.
Uzroci distrofije jetre
Steatoza se u pravilu javlja iz sljedećih razloga:
- Intoksikacija raznim hepatotropnim otrovima (otrovne gljive, žuti fosfor itd.);
- dijabetes;
- Često pijenje alkoholnih pića;
- Zloupotreba prehrambenih proizvoda koji sadrže ogromnu količinu konzervansa i masti;
- Gojaznost ili produženo gladovanje;
- Parenhimska proteinska distrofija;
- Nekontrolirana upotreba određenih lijekova;
- ovisnik o drogama;
- Tumori hipofize.
Klasifikacija
Prvo, na osnovu promjena u strukturi steatoze, bilježi se nekoliko vrsta jetrene distrofije:
- Zonska difuzija. Karakteriziraju ga lokalne masne formacije u određenim područjima jetre. Kliničke manifestacije su prilično jake.
- Diseminirana rasprostranjena distrofija. Masne formacije su u blizini i značajno su zbijene u ljudskoj jetri. Simptomi: opšta slabost i nelagodnost u desnom hipohondrijumu.
- Diseminirana fokalna distrofija. Karakteriziraju ga rijetke, tačkaste i nedosljedno locirane masne formacije. Simptomi nisu izraženi.
- difuzna distrofija. Ovu vrstu distrofije jetre karakterizira obilna količina masnih inkluzija, koje mogu biti na mjestu cijele jetre ili u jednom od njenih dijelova.
Osim toga, distrofija bubrega može se podijeliti u nekoliko faza ovisno o periodu razvoja bolesti:
- Prva faza - male masne formacije mogu se naći u stanicama jetre, koje gotovo da nemaju utjecaja na funkcije hepatocita;
- Druga faza - uočava se početak uništavanja jetre, odnosno hepatocita, a u blizini mrtvih ćelija mogu nastati male upale ili ciste.
- Treći stadijum - promjene na jetri se više ne mogu spriječiti, neki dijelovi jetre odumiru, uslijed čega se razvija ciroza jetre.
Šta je opasna distrofija jetre?
Distrofija jetre je zaista ozbiljna bolest, koja se ni u kom slučaju ne može previdjeti ili ne posvetiti dužnu pažnju specifičnim simptomima.
Stoga, ako osoba sa steatozom ne želi započeti liječenje, onda kasnije može očekivati:
- Povećan rizik od kardiovaskularnih bolesti i dijabetesa;
- hronični hepatitis;
- fibroza;
- ciroza;
- Nekroza jetre.
Da biste izbjegli ovako strašne posljedice, morate slušati svoje tijelo i biti svjesni znakova distrofije jetre.
Simptomi i znaci masne jetre
Pacijenti koji pate od metaboličkih poremećaja u stanicama jetre često nemaju pritužbi na svoje fizičko stanje, jer u početnim fazama hepatoza jetre teče bezbolno i izvana neprimjetno.
Bolest nestaje tokom prilično dugog perioda. S vremenom pacijent počinje osjećati nelagodu u obliku:
- tup bol u desnom hipohondrijumu;
- stalna slabost tijela;
- glavobolja;
- brza iscrpljenost tokom aktivnosti koje zahtijevaju fizičku aktivnost;
- vrtoglavica.
Najrjeđi slučaj je distrofija jetre sa jasno izraženim kliničkim simptomima. Od njih možemo razlikovati:
- oštar gubitak težine;
- oštar i nepodnošljiv bol;
- nadimanje.
Metode za dijagnosticiranje distrofije jetre
Postoje dva načina za otkrivanje lipodistrofije:
- Hemija krvi. Ova analiza lako ukazuje na povećanje broja specifičnih vrsta proteina (alanin aminotransferaza (ALT) i aspartat aminotransferaza (AST)), koji imaju svojstvo povećanja tokom distrofije jetre.
- Ultrazvuk abdomena. Odmah otkriva eho znakove hematoze i omogućava vam da odredite točnu dijagnozu.
- testovi jetre.
Liječenje bolesti
Prije nego što govorimo o lijekovima koji pomažu u ublažavanju simptoma i liječenju bolesti, treba napomenuti da bez pridržavanja određene dijete nijedan lijek neće djelovati u punom potencijalu i neće pomoći kako bismo željeli. Često je jedna dijetalna terapija dovoljna za oporavak.
Samo u slučaju da pravilna prehrana koju preporučuje liječnik ne pomaže u rješavanju distrofije jetre, treba uvesti medikamentozne metode liječenja. Iz širokog izbora lijekova za otklanjanje hepatoze jetre mogu se koristiti lijekovi koji doprinose:
- razgradnju masti
- uklanjajući ga iz tela.
Treba naglasiti da je potrebno ponavljati ovaj tretman više puta godišnje.
Bolesnoj osobi čije se stanje stabilizira upotrebom lijekova potrebno je i:
- vitaminska terapija,
- upotreba hepatoprotektora i antioksidanata koji poboljšavaju rad jetre, obavljaju zaštitnu funkciju u odnosu na ćelijske membrane,
- imunomodulatorni lijekovi koji jačaju tijelo.
Također, ako pacijent pati od ove bolesti istovremeno s gojaznošću, tada mu se preporučuje:
- postepeno smanjivati težinu (oko 1-1,5 kilograma sedmično),
- baviti se gimnastikom,
- razne vježbe usmjerene na sagorijevanje viška rezervi potkožnog tkiva.
Koju konkretnu fizičku aktivnost vrijedi raditi, svakako morate saznati od specijaliste iz oblasti medicine.
Dijeta za bolest
Prehrana za masnu hepatozu mora se pažljivo razmotriti tako da dnevna prehrana uključuje maksimalnu količinu zdrave bogate hrane:
Količina masti treba svesti na minimum.
Osnovna pravila prehrane za lipodistrofiju:
- Jedite najmanje sto grama proteina dnevno;
- Potpuno napustite alkoholna pića;
- 2/3 proteina mora biti životinjskog porijekla;
- Nemojte jesti veliku količinu hrane odjednom, odnosno jedite djelimično;
- Ne unosite više od dvadeset posto masti od ukupne količine hrane dnevno;
- Smanjite potrošnju konzervansa i purinskih supstanci.
Potrebno je detaljnije razmotriti prehranu i potrebnu hranu za hepatozu jetre.
- kuvano,
- na pari,
- pečeni u pećnici (na primjer, riba ili meso).
Također morate koristiti, i to prilično često, svježi sir i pavlaku s malim sadržajem:
Potrebno je odbiti zasićene juhe od povrća ili mesa. Važno je izbjegavati:
- masno meso i riba,
- pečurke,
- paradajz,
- proizvodi od pasulja,
- sirovi luk i beli luk
- razne dimljene i konzervirane hrane.
Važno je da pijete najmanje litar tečnosti dnevno, na primer:
- čista voda za piće,
- biljni dekoti,
- mleko itd.
- salate od povrća sa maslinovim uljem,
- supe od povrća ili mleka,
- kuvana šargarepa,
- kupus,
- razne žitarice (najbolje zobene pahuljice, heljda, griz i pirinač).
Prevencija
Najvažnija činjenica u prevenciji bolesti je poštivanje pravilne prehrane, koja uključuje potrebne komponente koje su bogate vitaminima i elementima u tragovima korisnim za jetru.
Također morate redovno prolaziti kroz posebne medicinske preglede, koji se provode u početnim razdobljima razvoja masne hepatoze. To će nesumnjivo pomoći u sprječavanju daljnjeg razvoja bolesti. Pogotovo u kasnijim fazama, mnogo je teže ispraviti situaciju, a ponekad je već nemoguće.
Pitanje što je distrofija jetre zanima mnoge pacijente koji se suočavaju sa sličnom dijagnozom. Kako objašnjavaju liječnici, riječ je o komi koja je nastala kao rezultat duboke inhibicije funkcionalnosti jetre. Distrofiju jetre (LP) izazivaju različite bolesti s kroničnim tokom, u kojima je oštećena žučna žlijezda.
Jetra je jedinstven organ koji igra važnu ulogu u metabolizmu lipida. Trigliceridi iz hrane ulaze u crijeva, gdje ih enzimi razgrađuju, a zatim ulaze u krvotok. Zajedno s krvlju, masti ulaze u jetru, gdje se pretvaraju u različite tvari neophodne za normalno funkcioniranje organizma.
Uz prekomjerno nakupljanje lipida dolazi do masne degeneracije u kojoj se koncentracija masti u organu povećava 10 puta. Sadržaj triglicerida može doseći više od 50% ukupnog volumena žlijezde, a normalno ova brojka ne prelazi 5%.
Uzroci bolesti
U većini slučajeva, DP nastaje zbog činjenice da se smanjuje odgovor hepatocita (ćelija jetre) na djelovanje inzulina. Inzulin je hormon koji prenosi glukozu do tjelesnih ćelija. Zbog činjenice da hepatociti ne reagiraju na djelovanje inzulina, dolazi do nedostatka glukoze u jetri. Glukoza je vrlo važna za normalno funkcioniranje stanica jetre, stoga, s nedostatkom tvari, počinju umirati. Pogođene ćelije se vremenom zamenjuju masnim tkivom. Kao rezultat toga dolazi do poremećaja funkcionalnosti jetre.
Hepatociti postaju imuni na djelovanje inzulina zbog genetskih patologija ili metaboličkih poremećaja. Izostanak normalne reakcije ćelija jetre može biti posljedica imunološke agresije u odnosu na inzulin.
Ostali uzroci DP-a:
- Prisustvo loših navika (alkohol, pušenje).
- Prekomjerna konzumacija masne hrane.
- Pasivni stil života.
Svi ovi faktori negativno utječu na stanje jetre, izazivajući nepovratne promjene.
Uradite ovaj test i saznajte imate li problema s jetrom.
Simptomi distrofije jetre najčešće su blagi i pacijent jednostavno ne obraća pažnju na njih. Pacijenti se u pravilu ne žale na bilo kakve uznemirujuće pojave. Patološki proces se razvija sporo, a klinička slika nije jasna.
Međutim, s vremenom se pojavljuju sljedeći simptomi:
- tup bol desno ispod rebara;
- hepatomegalija;
- mučnina;
- erupcija povraćanja;
- poremećaji stolice.
U rijetkim slučajevima, distrofične promjene u žlijezdi praćene su jakim bolom u trbuhu, naglim smanjenjem težine, svrbežom, žutilom kože i sluznica.
Obično se simptomi DP dijele prema vrsti patologije. S toksičnom distrofijom jetre s raširenom nekrozom (odumiranjem tkiva) parenhima organa, uočava se povećan rast hepatocita, koji se nalaze uz portalnu venu limfnih čvorova i slezene. DP se manifestuje višestrukim krvarenjem u koži, unutrašnjim i seroznim membranama. Osim toga, postoje nekrotične i distrofične promjene u tkivima koje zahvaćaju srčani mišić i gušteraču.
Lipodistrofija jetre
Masna degeneracija jetre (masna hepatoza) nastaje zbog zamjene hepatocita masnim stanicama. Kod hepatoze se nakupljaju masne naslage koje izgledaju kao kapi na jetri.
Uzrok masne degeneracije je patologija žučne kese, njenog kanala ili crijevnog trakta. ZhDP (masna jetra) može izazvati sljedeće bolesti:
- Teška gojaznost.
- Diabetes mellitus tip 2 malapsorptivni i maldigestivni sindrom.
- Prekomjerna konzumacija alkoholnih pića.
- Uzimanje kortikosteroida, tetraciklina, estrogena, NSAIL.
Lipodistrofija se često javlja na pozadini hepatitisa s kroničnim tijekom (posebno kod hepatitisa tipa C).
Makropreparat karakterističan za IDP: hepatomegalija, površina jetre je glatka, konzistencija je gusta ili mlohava, prednji rub organa je zaobljen, glinast, žut ili žuto-smeđi.
Toxic DP
Toksična distrofija jetre (TDP) se manifestuje ekstenzivnim brzo razvijajućim nekrotskim procesima koji utiču na strukturu jetre. Obično patologija ima akutni tijek, ali ponekad postaje kronična, izazivajući disfunkciju jetre.
Masivna nekroza se razvija pod uticajem toksina koji se nalaze u hrani, kao što su gljive. Takvo trovanje nastaje pod utjecajem vanjskih faktora. Toksična degeneracija jetre može nastati zbog endotoksikoze. Takva stanja uključuju toksikozu kod trudnica, hipertireozu (višak hormona štitnjače). Često se TDP javlja u pozadini hepatitisa, tada je distrofija simptom njegovog fulminantnog oblika.
Toksičnu distrofiju jetre prati hepatomegalija, mlohavost ili gustoća jetrenog tkiva, organ postaje žut. Ako se ne liječi, veličina žlijezde se smanjuje, kapsularna membrana postaje naborana. Orgulje poprimaju sivu boju i spolja podsjećaju na glinenu masu. Za 3 sedmice, žlijezda nastavlja da se smanjuje, njena boja se mijenja u crvenkastu. Vremenom počinje da se otkriva retikularna stroma jetre u kojoj su vidljive proširene, krvlju ispunjene kapilare. Ćelije jetre su očuvane samo u određenim područjima lobula. Ovako se manifestuje crvena distrofija.
Hronični TDP je rijetko stanje u kojem je vjerojatnije da će pacijent umrijeti zbog brzo progresivne disfunkcije jetre.
Akutna distrofija jetre
Akutna distrofija jetre (ALP) najčešće je komplikacija hepatitisa A, koji se javlja u nepovoljnom obliku. Zasebno, patologija se razvija prilično rijetko.
Bolest je malo proučavana, tako da doktori ne mogu tačno odgovoriti kako se razvija. Također nije jasno da li postoji veza sa jačinom virusa ili neki drugi faktori utiču na patološki napredak.
Otežani parenhimski hepatitis provociran je sljedećim bolestima: bruceloza, krpeljna povratna groznica, sifilis. Osim toga, povećava se vjerojatnost komplikacija bolesti tijekom trudnoće ili nakon pobačaja. Ovi faktori negativno utiču na ćelije jetre, izazivajući tešku distrofiju.
Simptomi ADP-a u ranoj fazi su slični onima kod hepatitisa A, pa postoji rizik od značajnog pogoršanja stanja pacijenta. Patološki proces utječe na nervni sistem, kao rezultat toga, aktivnost mozga je poremećena. Bolest se manifestuje delirijumom, anksioznošću, konvulzijama, erupcijom povraćanja. U tom slučaju pacijent mora biti hitno hospitaliziran na psihijatrijskom odjelu.
Moguća je i obrnuta reakcija nervnog sistema: ravnodušnost prema svemu što se dešava, depresija, smanjenje vitalnosti, žudnja za snom. Simptomi nastavljaju da rastu, pacijent gubi svijest, razvija se hepatična koma.
Alkoholna distrofija
Ova vrsta distrofije nastaje zbog prekomjernog pijenja 10-12 godina. Etilni alkohol prodire u organizam i truje hepatocite.
Alkoholna distrofija jetre (ALD) može se pojaviti u pozadini hepatoze, ciroze, alkoholnog hepatitisa. Najčešće je hepatoza ta koja uzrokuje distrofiju žlijezde zbog prekomjernog pijenja. Ako pacijent odbije jaka pića u ranoj fazi hepatoze, stanje jetre se poboljšava nakon 2-4 tjedna. U većini slučajeva, ADP ne pokazuje teške simptome.
- Povećanje parotidnih pljuvačnih žlezda.
- Fleksijska kontraktura prstiju.
- Crvenilo dlanova, a ponekad i stopala.
Najlakši način za identifikaciju bolesti su laboratorijske pretrage i biopsija.
Difuzna distrofija
Difuzne distrofične promjene u parenhima jetre su vrlo opasno stanje. Nastaje kao rezultat činjenice da hepatociti nisu u stanju neutralizirati toksine koji ulaze u tijelo. Stanice jetre ne mogu se nositi s velikim trovanjem, zbog čega parenhimsko tkivo počinje odumirati, a fibrozno vezivno tkivo raste u oštećenim područjima. Difuzne promjene su sve izraženije, a to prijeti zatajenjem jetre. Ovako se manifestuje difuzni DP.
Degenerativne distrofične promjene u jetri najčešće izazivaju sličan proces u pankreasu. To je zbog činjenice da su ti organi usko povezani jedni s drugima.
Fokalna distrofija
Fokalnu distrofiju jetre (OLD) teško je otkriti laboratorijskim testovima. To je prilično teško čak i unatoč činjenici da postoje funkcionalni poremećaji žlijezde. Simptomi bolesti ovise o uzrocima koji su je izazvali.
Fokalnom transformacijom zahvaćeni su pojedini dijelovi jetre
Fokalni DP, koji je nastao kao posljedica prekomjerne konzumacije alkoholnih pića, manifestuje se otežanim disanjem, gubitkom apetita, ponekad se javlja bol na desnoj strani ispod rebara. Ovi znakovi postaju izraženiji kada se pacijent kreće.
Najefikasnije metode za otkrivanje patologije su magnetna rezonanca i kompjuterska tomografija.
Granularna distrofija
Ovo je najčešći tip proteina DP. Granularnu distrofiju jetre (GLD) karakterizira kršenje koloidnih svojstava citoplazme stanice, u kojoj se pojavljuje protein sličan zrnu.
ZDP izazivaju sljedeći faktori:
- Neadekvatno hranjenje novorođenčeta.
- Intoxication.
- Zarazne bolesti.
- Poremećaj cirkulacije krvi i cirkulacije limfe.
- Uzroci koji izazivaju gladovanje tkiva kiseonikom.
Vremenom se kod ZDP-a mijenja metabolizam proteina u stanicama, citoplazma postaje zamućena, bubri. Zbog oštećenja jetrenog tkiva, žučna žlijezda postaje mlohava, poremećena je njena prokrvljenost.
Važno je razlikovati znakove RDD od prirodnih procesa sinteze proteina u ćelijama, u kojima se pojavljuje granularnost proteina.
Ova patologija je reverzibilna, ali ima težak tok. Stoga postoji mogućnost degeneracije ZDP-a u intracelularnu hijalinozu, vodenicu ili nekrozu.
Protein DP
Proteinska degeneracija jetre (BDP) nastaje kao rezultat poremećaja metabolizma proteina i javlja se u pozadini amiloidoze, hijalinske ili granularne degeneracije.
Kod amiloidoze, amiloid (kompleks protein-polisaharid) se formira i deponuje u tkivima.
Uz BDP, jetra poprima granularnu strukturu, budući da se u protoplazmi stanica pojavljuju kapljice i zrnate formacije. Kombiniraju se i ispunjavaju unutarćelijski prostor. Proteinske strukture postaju gušće, rad stanica žlijezde je poremećen, kao rezultat toga, tkiva jetre umiru.
hidropična distrofija
Hidropična degeneracija jetre (HDP, vakuolna degeneracija) je praćena pojavom vakuola (šupljine u ćelijskoj citoplazmi), koje su ispunjene citoplazmatskom tečnošću. U patologiji se povećavaju ćelije parenhima organa, što je praćeno naboranjem ili vakuolizacijom jezgra.
Kako bolest napreduje, jetra se preplavljuje tekućinom, a njene ultrastrukture se razlažu. Pogođene ćelije izgledaju kao posude ispunjene vodom i predstavljaju kontinuiranu šupljinu sa jezgrom u obliku mjehurića. Ovako se manifestuje BDP.
Promjene se mogu otkriti samo mikroskopom, jer se jetra ne mijenja spolja.
Žuta distrofija jetre
IRL je često komplikacija trudnoće. Patologija nastaje kao rezultat akutnog trovanja tijela u pozadini zaraznih bolesti. Žuticu kod buduće majke može izazvati DP, upala žučne kese, kamenac u jetri. Osim toga, bolest se može pojaviti samostalno zbog autointoksikacije tijela (toksikoze).
IDP je težak stepen toksikoze kod trudnica. Patologija nastaje zbog teškog trovanja metabolitima. Bolest se manifestuje žutim bojenjem kože i sluzokože, obilnim povraćanjem, zamućenjem svijesti, delirijumom i povećanom razdražljivošću. Osim toga, postoji mogućnost hemoragijskog osipa (krvarenja pod kožom), smanjuje se volumen mokraće, sadrži cirozin i lecitin, smanjuje se tupost jetre. Ako se ne liječi, pacijent umire u roku od nekoliko dana.
Dijagnoza bolesti
Dijagnoza DP je teška, jer su tradicionalne laboratorijske pretrage neefikasne, unatoč disfunkciji žlijezde.
Bolest je obično asimptomatska, jedini znak patologije je hepatomegalija. Ehogenost jetre tokom ultrazvuka ostaje u granicama normale, a ponekad se čak i povećava, pa je prilično teško razlikovati DP od ciroze ili fibroze. Ultrazvučni pregled otkriva područja sa povećanom ehogenošću. Područja niske ehogenosti mogu se identificirati pomoću CT-a. Kompjuterska i magnetna rezonanca su najinformativnije metode za prepoznavanje DP. Uz njihovu pomoć moguće je odrediti žarišnu hepatozu jetre.
Biopsija se radi za otkrivanje patologije. Patomorfološkim pregledom tkiva lekar će utvrditi višak nakupljanja masti.
Metode liječenja
Mnogi pacijenti se pitaju kako liječiti DP. Liječenje se sastoji u pridržavanju sljedećih pravila:
- Dijeta.
- Liječenje pratećih bolesti.
- Obnova strukture jetre.
- Konsolidacija rezultata.
Lekari po pravilu propisuju sledeće lekove:
- hepatoprotektori,
- sintetički antioksidansi,
- statini.
Hepatoprotektori stabiliziraju ćelijske membrane, vraćaju njihov integritet. Poboljšavaju metabolizam bilirubina, masnih kiselina, proteina. U tu svrhu koriste se Karsil, LIV-52, Hofitol, Essentiale itd.
Koleretici poboljšavaju lučenje žuči, normaliziraju njen sastav i smanjuju začepljenje. Uz DP, Allohol, Holosa su propisani.
Statini koriguju lipidni profil krvi. Uz njihovu pomoć smanjuje se prodiranje masti u krvotok, a višak kolesterola se izlučuje iz tijela.
Ako se kod DP uoči hepatična encefalopatija, pacijent se hitno hospitalizira. Pacijentu se daju lijekovi parenteralnom metodom, ograničiti količinu proteina. Osim toga, propisuju se lijekovi koji koriguju acido-bazno stanje. Acidoza se često manifestira kod DP-a, a da bi se spriječila primjenjuje se natrijum bikarbonat. Antibakterijski agensi suzbijaju crijevnu mikrofloru.
Kod funkcionalnih poremećaja jetre propisana je ekstrakorporalna enterosorpcija. Glukokortikoidi se koriste za potporu metabolizma.
Da biste smanjili opterećenje jetre i ubrzali oporavak, potrebno je revidirati jelovnik. Dijeta treba uključivati hranu koja sadrži vitamine, vlakna, pektine, ugljikohidrate. Dnevna norma masti je 70 g. Važno je isključiti hranu koja sadrži holesterol i ograničiti unos soli.
Prilikom liječenja DP-a zabranjeno je piti kafu, čaj, sokove i alkohol.
Pacijentima je dozvoljeno da jedu supe sa povrćem, žitaricama ili na bazi obranog mleka. Preporučuje se konzumiranje svežeg, kuvanog, pečenog ili parenog povrća. Povremeno možete uživati u nemasnoj šunki, tvrdom siru (ne ljutom), omletu od belanaca ili kuvanim jajima (ne više od 1 jajeta dnevno). U ishranu možete uključiti i heljdu, zobene pahuljice, griz i pirinač. Osim toga, kiselo mliječni proizvodi s niskim postotkom masti nisu zabranjeni.
Preventivne mjere i prognoza za DP
Da biste spriječili bolest, trebate izbjegavati faktore koji je izazivaju. Važno je odreći se loših navika: alkohola, pušenja, prekomjerne konzumacije hrane (posebno masne), pasivnog načina života.
Da biste održali visoku vitalnost i spriječili razvoj patoloških procesa, trebali biste jesti ispravno, ograničiti upotrebu vruće, pržene hrane, dimljenih, konzerviranih proizvoda. Osim toga, pacijent treba stalno pratiti težinu i održavati je u granicama normale.
Da bi jetra normalno funkcionisala, svakodnevno se treba baviti sportom: hodanjem, trčanjem, plivanjem itd.
Ako DP nije praćen drugim bolestima, onda je prognoza povoljna. Kod distrofije s izraženim komplikacijama, imunitet se smanjuje, tijelo postaje osjetljivo na zarazne bolesti. Patogeni mikrobi ulaze u organizam, kao rezultat toga, pacijent podnosi anesteziju, lošije kirurške zahvate i duže se oporavlja nakon njih.
Ako pacijent vodi pogrešan način života i ne pristupi liječenju, onda patologija napreduje. Tada se povećava vjerovatnoća male nodularne ciroze, nealkoholnog steatohepatitisa.
Ako je tokom liječenja DP-a pacijent odbio alkohol, slijedi dijetu i preporuke liječnika, tada će najvjerovatnije moći održati radnu sposobnost i poboljšati svoje opće stanje.
Na osnovu navedenog, distrofija jetre je opasna bolest s kroničnim tijekom, koja nastaje kao rezultat duboke inhibicije funkcionalnosti žlijezde. Kako biste spriječili opasne komplikacije, morate paziti na svoje zdravlje i, ako se pojave sumnjivi simptomi, kontaktirati hepatologa ili gastroenterologa. Ukoliko je potrebno, lekar će propisati ultrazvuk, magnetnu rezonancu ili CT, kao i biopsiju. Pacijent mora striktno slijediti preporuke liječnika i voditi zdrav način života.
U kontaktu sa
Distrofija- (od grč. dys - kršenje, trofe - ishrana) - kvalitativne promjene u hemijskom sastavu, fizičko-hemijskim svojstvima i morfološkom tipu ćelija i tkiva u tijelu povezane s metaboličkim poremećajima. Promjene u metabolizmu i strukturi ćelije, koje odražavaju prilagodljivu varijabilnost tijela, nisu povezane s distrofičnim procesima.
Etiologija.
Poremećaj metaboličkih procesa, koji dovodi do strukturnih promena u tkivima, uočava se pod uticajem mnogih spoljašnjih i unutrašnjih faktora (biološki neadekvatna ishrana, različiti uslovi držanja i eksploatacije životinja, mehanička, fizička, hemijska i biološka dejstva, infekcije, intoksikacije, poremećaji cirkulacije krvi i limfe, lezije endokrinih žlezda i nervnog sistema, genetske patologije itd.). Patogeni faktori djeluju na organe i tkiva direktno ili refleksno kroz neurohumoralni sistem koji reguliše metaboličke procese. Priroda distrofičnih procesa ovisi o jačini, trajanju i učestalosti izlaganja određenom patogenom stimulusu na tijelu, kao i o reaktivnom stanju organizma i vrsti oštećenog tkiva. U suštini, distrofične promjene se bilježe kod svih bolesti, ali se u nekim slučajevima javljaju primarno i određuju prirodu bolesti, dok su u drugima nespecifičan ili sekundarni patološki proces koji prati bolest.
Patogeneza
. Savremene metode istraživanja (histohemijske, elektronsko mikroskopske, autoradiografske, biohemijske itd.) pokazale su da se svaki distrofični proces zasniva na kršenju enzimskih reakcija (fermentopatija) u metabolizmu (sintezi i raspadu) supstanci sa oštećenjem (promenom) struktura i funkcije ćelijsko - tkivnih sistema organizma. Istovremeno se u tkivima akumuliraju produkti metabolizma (promijenjeni i kvantitativno i kvalitativno), fiziološka regeneracija (obnova žive tvari, prvenstveno na molekularnom i ultrastrukturnom nivou njene organizacije) i funkcije jednog ili drugog organa, kao i vitalna aktivnost organizma u cjelini, poremećena je.
Razvojni mehanizam
i suština promjena kod različitih distrofija nije ista.
Prema mehanizmu procesa distrofičnih promjena razlikuju se: razgradnja; infiltracija; transformacija i izmijenjena ili izopačena sinteza.
Razgradnja (od latinskog decompositio - restrukturiranje) - promjena ultrastrukture, makromolekula i složenih (protein-masno-ugljikohidratnih i mineralnih) spojeva ćelijskog i tkivnog sistema. Neposredni uzroci ovakvog restrukturiranja su neravnoteža nutrijenata, metabolita i metaboličkih produkata, hipoksija i intoksikacija, promjene temperature (groznica, prehlade), kiselinsko-bazni disbalans (acidoza, rjeđe alkaloza), redoks i elektrolitni potencijal stanica i tkiva. . Kao rezultat promjena u osnovnim parametrima ćelijsko-tkivnih sistema (pH, stanje ATP sistema, itd.), složena biološka jedinjenja ćelijskih organela i makromolekula se mijenjaju ili raspadaju u jednostavnija jedinjenja koja postaju dostupna za histohemijsko proučavanje. Slobodni proteini se hidroliziraju uz sudjelovanje enzima lizosoma ili podliježu denaturaciji. U tom slučaju, uz primarno oštećenje ultrastrukture, mogu se pojaviti sekundarni procesi (na primjer, stvaranje kompleksnih spojeva kao što su amiloid, hijalin itd.).
Patološka infiltracija(od lat. infiltratio - impregnacija) karakteriše taloženje i nakupljanje (taloženje) u ćelijama i tkivima metaboličkih produkata (proteina, lipida, ugljenih hidrata itd.) i supstanci koje se unose krvlju i limfom („bolesti skladištenja“) ,
Transformacija (od latinskog transformatio - transformacija) je proces hemijske transformacije jedinjenja u druge, na primjer masti i ugljikohidrata u proteine ili proteina i ugljikohidrata u masti, povećana sinteza glikogena iz glukoze, itd., uz prekomjerno nakupljanje novoformiranih spojeva.
Modified Synthesis bilo koje jedinjenje se izražava u povećanom ili smanjenom stvaranju istih sa akumulacijom ili iscrpljivanjem i gubitkom u tkivima, kao što su glikogen, mast, kalcijum, itd. ("bolest nedostatka"). „Izopačena“ (patološka) sinteza je moguća pojavom i akumulacijom u tkivima jedinjenja koja nisu karakteristična za njih u normalnim metaboličkim uslovima, na primer, sinteza neobičnog amiloidnog proteina, glikogena u epitelu bubrega, keratina u epitelu suzne žlijezde, patološki pigmenti itd.
Ovi patogenetski mehanizmi distrofija mogu se manifestirati istovremeno ili uzastopno kako se proces razvija.
Morfološki distrofije se manifestiraju prvenstveno kršenjem strukture ultrastruktura stanica i tkiva. U fiziološkim uslovima, restrukturiranje ćelijskih organela i međućelijske supstance se kombinuje sa procesima njihove obnove, a kod distrofija je poremećena regeneracija na molekularnom i ultrastrukturnom nivou (molekularna morfogeneza). Kod mnogih distrofija u ćelijama i tkivima se nalaze inkluzije, zrnca, kapi ili kristali različite hemijske prirode, koji se u normalnim uslovima ne javljaju ili se njihov broj povećava u odnosu na normu. U drugim slučajevima, naprotiv, u ćelijama i tkivima broj spojeva karakterističnih za njih opada do potpunog nestanka (glikogen, masti, minerali itd.). U oba slučaja ćelije i tkiva gube svoju karakterističnu finu strukturu (mišićno tkivo - poprečna prugasta, žljezdane ćelije - polaritet, vezivno tkivo - fibrilarna struktura itd.), a u težim slučajevima uočava se diskompleksacija ćelijskih elemenata (npr. poremećena gredna struktura jetre).
makroskopske promene.
Kod distrofije se mijenja boja, veličina, oblik, tekstura i uzorak organa. Promjena izgleda organa poslužila je kao osnova da se ovaj proces nazove ponovnim rođenjem, odnosno degeneracijom - termin koji ne odražava suštinu distrofičnih promjena.
Funkcionalna vrijednost distrofija.
Sastoji se od kršenja osnovnih funkcija organa (na primjer, sinteza proteina, ugljikohidrata, lipoproteina u hepatozi, proteinurija u nefrozi, slabljenje srčane aktivnosti kod distrofije miokarda itd.). Nakon otklanjanja uzroka koji je izazvao razvoj distrofičnog procesa, metabolizam u stanicama, tkivima i cijelom organizmu u pravilu se normalizira, zbog čega organ dobiva funkcionalnu korisnost i normalan izgled. Međutim, teške distrofične promjene su ireverzibilne, odnosno sve veći disproporcija između pojačanog raspada vlastitih struktura i nedovoljne restauracije završava se njihovom nekrozom.
PROTEINSKA DISTROFIJA (disproteinoza)
Proteinske distrofije- Strukturni i funkcionalni poremećaji tkiva povezani sa promjenama u hemijskom sastavu, fizičko-hemijskim svojstvima i strukturnoj organizaciji proteina. Nastaju kada postoji neravnoteža između sinteze i razgradnje proteina u ćelijama i tkivima kao posledica nedostatka proteina ili aminokiselina, kada organizmu strane materije dospeju u tkiva, kao i tokom patološke sinteze proteina. Poremećaji metabolizma proteina u organizmu su raznovrsni. Mogu imati lokalnu ili opštu (sistemsku) distribuciju. Lokalizacijom se javljaju poremećaji metabolizma proteina u ćelijama (ćelijske, ili parenhimske, disproteinoze), u međućelijskoj supstanci (ekstracelularne, odnosno stromalno-vaskularne, disproteinoze) ili istovremeno u ćelijama i međućelijskoj supstanci (mešovite disproteinoze).
ĆELIJA (PARENHIMATOZNA) DISPROTEINOZA
Granularna distrofija ili mutni otok, - kršenje koloidnih svojstava i ultrastrukturne organizacije ćelija uz detekciju proteina u obliku zrna. Ovo je najčešći tip proteinske distrofije.
Razlozi: zarazne i parazitske bolesti, pothranjenost i intoksikacija, poremećaji cirkulacije krvi i limfe i drugi patogeni faktori.
Patogeneza komplikovano. Vodeći mehanizam je razgradnja, koja se zasniva na insuficijenciji ATP sistema povezanom sa hipoksijom, dejstvom toksičnih supstanci na enzime oksidativne fosforilacije (fermentopatija). Kao rezultat, smanjuje se redoks potencijal stanica, akumuliraju se podoksidirani i kiseli (acidoza), rjeđe alkalni (alkaloza) metabolički produkti, povećavaju se onkotičko-osmotski tlak i propusnost membrane. Poremećaj razmene elektrolita i vode praćen je oticanjem ćelijskih proteina, narušavanjem stepena disperzije koloidnih čestica i stabilnosti koloidnih sistema, posebno u mitohondrijama. Istovremeno se povećava aktivnost hidrolitičkih enzima lizosoma. Hidrolaze razbijaju intramolekularne veze dodavanjem molekula vode, uzrokujući preuređenje kompleksnih spojeva i makromolekula. Adsorpcija bilo koje toksične tvari u kompleksima lipoproteina i glikoproteina također uzrokuje njihovo restrukturiranje i dezintegraciju. Oslobođeni protein, a zatim i ostale komponente kompleksnih jedinjenja (masti i sl.) postaju grublje i u izoelektričnom stanju koaguliraju sa pojavom zrna. U tom slučaju može biti poremećena sinteza citoplazmatskog proteina (molekularna morfogeneza), što se pokazalo uz pomoć obilježenih atoma (S. V. Anichkov, 1961).
Uz razgradnju, pojava granularnosti povezana je i s patološkom transformacijom ugljikohidrata i masti u proteine, infiltracijom i resorpcijom tijela stranih proteina (paraproteina) koje donosi krvotok (disproteinemija).
Histološke karakteristike granularna distrofija je najizraženija u jetri, bubrezima, miokardu, a takođe iu skeletnim mišićima (zato se naziva i parenhimskom). Primjećuju neravnomjerno povećanje volumena epitelnih stanica i mišićnih vlakana koja komprimiraju kapilare, oticanje i zamućenje citoplazme, glatkoću i nestanak fine strukture (četkasta ivica žljezdanog epitela, poprečna pruga u mišićnom tkivu itd.), pojava i akumulacija u citoplazmi male acidofilne granularnosti proteina. U isto vrijeme, granice ćelija i obrisi jezgara teško se razlikuju. Ponekad citoplazma poprima pjenasti izgled, neke ćelije se odvajaju od bazalne membrane i jedna od druge (diskompleksacija). Pod utjecajem slabe otopine octene kiseline ili lužine, citoplazma postaje bistra, jezgro ponovo postaje vidljivo. Uz rastvorljivost u slabim kiselinama i alkalijama, histohemijskim metodama, kao i elektronskim mikroskopom, utvrđuje se prisustvo proteina u zrnu.
Elektronski mikroskopski granularnu distrofiju karakterizira oticanje i zaokruživanje mitohondrija, širenje cisterni i tubula citoplazmatskog retikuluma. Mitohondrije se povećavaju, njihove membrane se rastežu, raslojavaju, kapice se neravnomjerno debljaju i skraćuju, strukturni proteini mitohondrija se rastvaraju bistrenjem matriksa i pojavom prozirnih vakuola (mitohondrijska vakuolizacija) ili bujaju i povećavaju se. Aparat ćelije za sintezu proteina (polizomi, ribozomi) se takođe raspada.
Makroskopski zahvaćeni organi su uvećani, mlohave konzistencije, anemični, na rezu tkivo otiče izvan kapsule, površina reza je tupa, jetra i bubrezi su sivkasto-smeđe boje sa zaglađenom šarom, a mišićno tkivo (miokard, skeletni mišići) nalikuje na meso opečeno kipućom vodom.
Klinički značaj granularna distrofija je u tome što su funkcije zahvaćenih organa poremećene i mogu se kvalitativno promijeniti (slabost srca kod zaraznih bolesti, albuminurija kod oštećenja bubrega itd.).
Exodus zavisi od mnogo razloga. Zrnasta distrofija je jedan od reverzibilnih procesa, ali ako se ne otklone njeni uzroci, onda na vrhuncu razvoja može prerasti u teži patološki proces - u hidropičnu, hijalinsko-kapljičnu, masnu i druge vrste distrofija sa ishodom u ćelijska nekroza (tzv. acidofilna degeneracija)., "balon" distrofija ili koagulativna nekroza).
Diferencijalna dijagnoza. Granularnu distrofiju treba razlikovati od fiziološke sinteze proteina u ćeliji s akumulacijom proteinske granularnosti povezane s normalnim funkcioniranjem tijela (na primjer, stvaranje granula sekrecije u žljezdanom organu) ili fiziološkom resorpcijom proteina od strane ćelija (na primjer, u bubrežnim tubulima proksimalnog segmenta). Ovaj intravitalni proces razlikuje se od postmortalnih promjena organa (kadaverična tupost) po jasno izraženom povećanju veličine ćelija i organa, kao i po neujednačenosti patoloških lezija.
Hijalinska kap distrofija(od grčkog hyalos - staklast, proziran) - intracelularna disproteinoza, koju karakterizira pojava u citoplazmi prozirnih oksifilnih proteinskih kapi.
razlozi: akutne i kronične infekcije, intoksikacije i trovanja (živin hlorid, soli hroma, uranijuma itd.); osim toga, distrofija može biti rezultat alergijskih procesa nakon prethodne senzibilizacije proteina. Primjećuje se i kod kroničnih katara gastrointestinalnog trakta, mokraćne bešike, kod aktinomikoma i tumora.
Patogeneza- hijalin-kap distrofija se sastoji u činjenici da u patološkim stanjima dolazi do duboke denaturacije citoplazmatskih lipoproteina uz taloženje grube dispergirane faze zbog gubitka hidrofilnih svojstava proteina. U drugim slučajevima moguća je resorpcija i patološka infiltracija ćelije grubo dispergovanim proteinima stranim telu - paraproteinima koji dolaze iz krvi.
Makroskopski distrofija hijalinskih kapi nije dijagnosticirana.
Histološke promjene nalazi se u žlezdanim organima (jetra i dr.), tumorima, mišićnom tkivu, kao i u žarištima hronične upale, ali posebno često u epitelu tubula bubrega. Istovremeno, u citoplazmi su vidljive manje-više homogene, prozirne proteinske kapi, obojene kiselim bojama (na primjer, eozinom). Kako se kapljice akumuliraju i spajaju jedna s drugom, one mogu potpuno ispuniti ćeliju. Najteže promjene se javljaju kod glomerulonefritisa i proteinske nefroze u epitelu uvijenih tubula. Slične promjene se javljaju u epitelu nadbubrežnih žlijezda i bronhija. U kronično upaljenim tkivima, uglavnom u plazmocitima, takozvanim Russelovim, ili fuksinofilnim, nalaze se tijela u obliku velikih homogenih, ponekad slojevitih hijalinskih kuglica, koje su intenzivno obojene fuksinom i nakon propadanja ćelije slobodno leže u tkivu. . Elektronsko-mikroskopski zabilježite pojavu hijalinskih kapi i vakuola u citoplazmi, oticanje i propadanje mitohondrija, nestanak polisoma i ribozoma, rupture mrežnih cisterni itd.
Klinički značaj hyaline-drop distrofija jer odražava izraženu insuficijenciju organa, posebno bubrega.
Exodus. U vezi sa ireverzibilnom denaturacijom proteina plazme, distrofija hijalinskih kapi nastavlja sa ishodom nekroze.
Hidropična (hidropična, vakuolna) distrofija- kršenje metabolizma proteina-voda-elektrolita ćelije sa oslobađanjem vode unutar ćelija.
razlozi: infektivne bolesti (sat i šapa, male boginje, virusni hepatitis i dr.), upalne infiltracije tkiva, fizički, hemijski i akutni toksični efekti koji uzrokuju hipoksiju i razvoj edema, metaboličke bolesti (nedostatak proteina, gladovanje soli, hipovitaminoza, kao što je pelagra, itd.), kao i hronične intoksikacije i iscrpljenosti (hronični gastroenteritis, kolitis, itd.).
Patogeneza. Kao rezultat smanjenja oksidativnih procesa, nedostatka energije i nakupljanja nepotpuno oksidiranih metaboličkih produkata, vezana voda ne samo da se oslobađa i zadržava u ćeliji (intracelularna voda), već ulazi u ćeliju i iz tkivne tekućine (ekstracelularna). voda) zbog povećanja koloidno-osmotskog pritiska i poremećene permeabilnosti ćelijskih membrana. Istovremeno, ioni kalija napuštaju ćeliju, dok ioni natrija intenzivno prodiru u nju zbog narušavanja procesa osmoze povezanih s "jonskom pumpom". Biohemijska suština distrofija je aktivacija hidrolitičkih enzima lizosoma (esteraze, glukozidaze, peptidaze itd.), koji dodavanjem vode razbijaju intramolekularne veze, izazivajući hidrolizu proteina i drugih jedinjenja.
Histološke promjenečesto se instalira u epitelnom tkivu kože, jetri, bubrezima, nadbubrežnim žlijezdama, u nervnim stanicama, mišićnim vlaknima i leukocitima. Pokazuju znakove granularne distrofije, djelomičnu citolizu sa stvaranjem vakuola u citoplazmi (vakuolna distrofija) ispunjenih tekućinom koja sadrži proteine i enzime. Ponekad se protein citoplazmatske tekućine koagulira pod utjecajem kalcijevih soli. Daljnje otapanje citoplazme i povećanje količine vode u njoj izazivaju izraženiji intracelularni edem, čiji razvoj može dovesti do kariocitolize. U isto vrijeme, stanica se povećava, jezgro i citoplazma se rastvaraju, ostaje samo njena ljuska. Ćelija ima oblik balona (balonska distrofija). Elektronski mikroskopski zabilježite širenje i rupture tankova i tubula, oticanje i lizu mitohondrija, ribozoma i drugih organela, kao i otapanje glavne plazme.
Makroskopski organi i tkiva se malo mijenjaju, osim njihovog otoka i bljedila. Vakuolna distrofija se utvrđuje samo pod mikroskopom.
Klinički značaj hidropična distrofija u kojoj se funkcije zahvaćenog organa smanjuju.
Exodus. Vakuolna degeneracija je reverzibilna pod uslovom da ne dođe do potpunog rastvaranja citoplazme ćelije. Uz očuvanje jezgra i dijela citoplazme, normalizacija metabolizma vode-proteina i elektrolita dovodi do obnove stanice. Uz značajno uništenje organela s razvojem jakog edema (balon distrofija), dolazi do nepovratnih promjena (kolikvaciona nekroza).
Vakuolnu degeneraciju treba razlikovati od masne degeneracije histohemijskim metodama za određivanje masti, jer se u procesu proizvodnje histoloških preparata pomoću rastvarača (alkohol, eter, ksilen, hloroform) ekstrahuju masne supstance i na njihovom mestu se pojavljuju vakuole.
Horny distrofija ili patološka organizacija- prekomjerno (hiperkeratoza) ili kvalitativno poremećeno (parakeratoza, hipokeratoza) stvaranje rožnate tvari. Keratin boji ružičastu eozinom i žutu pikrofuksinom prema Van Giesonu. Ima osmiofilnost i visoku gustinu elektrona.
razlozi: metabolički poremećaji u organizmu - proteinski, mineralni (nedostatak cinka, kalcijuma, fosfora) ili nedostatak vitamina (hipovitaminoza A, posebno kod ptica, goveda i svinja, pelagra itd.); zarazne bolesti povezane s upalom kože (dermatofitoza, šuga, krasta itd.); fizički i hemijski iritirajući efekti na sluzokože i kožu; kronična upala sluznice; ponekad nasljedne bolesti (ihtioza - stvaranje rožnatih slojeva na koži, nalik ribljim krljuštima ili oklopu kornjače). Prekomjerno formiranje rogova se uočava kod bradavica, kankroida (kancerogenog tumora) i dermoidnih cista.
Patogeneza Horni distrofija je povezana s prekomjernom ili poremećenom sintezom kerotena u epidermisu kože i u keratiniziranom epitelu sluznice. Formiranje rožnate tvari u sluznicama probavnog trakta, gornjih dišnih puteva i genitalnih organa je praćeno zamjenom žljezdanog epitela keratinizirajućim pločastim višeslojnim epitelom.
Parakeratoza(od grčkog para - oko, keratos - rožnata supstanca) izražava se u gubitku sposobnosti epidermalnih ćelija da proizvode keratohijalin.
Histološki kod parakeratoze otkriva se zadebljanje epiderme kao rezultat hiperplazije stanica malpigijevog sloja i prekomjernog nakupljanja rožnate tvari. U sluzokožama tipa kože i u epidermi kože moguće je papilarno zadebljanje epiderme zbog hiperplazije sloja stiloidnih ćelija i izduženja stiloidnih procesa. Takve lezije se nazivaju akantoza (od grčkog akantha - trn, igla).
Kod para- i hipokeratoze izražena je atrofija granularnog sloja, stratum corneum je labav, sa diskompleksiranim ćelijama koje imaju štapićasta jezgra (nepotpuna keratinizacija).
Makroskopski na mjestima patološke keratinizacije (uobičajene ili lokalne) koža je zadebljana, s prekomjernim rastom stratum corneuma. Gubi elastičnost, postaje grub i tvrd, stvaraju se suva zadebljanja i žuljevi. Kod parakeratoze, stratum corneum je zadebljan, labav, uz pojačanu deskvamaciju stratum corneuma, a ponekad i gubitak kose. Kod odraslih životinja, posebno mliječnih krava, primjećuje se nenormalan rast kopitnog roga, koji gubi glazuru i puca.
Kod leukoplakije (od grčkog leukos - bijeli, plax, axos - ploča) na sluznicama formiraju se žarišta keratiniziranog epitela različitih veličina u obliku visokih niti i sivo-bjelkastih plakova.
Klinički značaj patološka keratinizacija povezana je s razvojem infektivnih komplikacija. Leukoplakija može postati izvor razvoja epitelnih tumora (papiloma, rijetko karcinoma).
Exodus horna distrofija zavisi od toka osnovne bolesti. Kada se otkloni uzrok koji uzrokuje patološku keratinizaciju, oštećeno tkivo se može obnoviti. Novorođene životinje koje boluju od ihtioze obično uginu prvog dana života.
VANSTANIČNA (STROMA-VASKULARNA) DISPROTEINOZA
To su kršenja metabolizma proteina u međućelijskoj tvari. Njihova suština leži u patološkoj sintezi proteina stanicama mezenhimskog porijekla, u dezorganizaciji (propadanju) osnovne tvari i vlaknastih struktura uz povećanje propusnosti vaskularnog tkiva i nakupljanje u međućelijskoj tvari vezivnog tkiva proteina krvi i limfe. , kao i metaboličkih proizvoda. Ovi procesi mogu biti lokalni ili široko rasprostranjeni. To uključuje mukoidno oticanje, fibrinoidno oticanje (fibrinoid), hijalinozu i amiloidozu.
Mukoidno oticanje- početna faza dezorganizacije vezivnog tkiva (stroma organa, krvnih žila), koju karakterizira kršenje veze s proteinima i preraspodjela kiselih glikozaminoglikana (hijaluronska, hondroitinsulfurna kiselina, itd.).
razlozi: gladovanje kiseonikom, intoksikacija, neke metaboličke bolesti (hipovitaminoza C, E, K) i endokrinog sistema (miksedem), alergijske akutne i hronične bolesti vezivnog tkiva i krvnih sudova („kolagene bolesti“, reumatizam, ateroskleroza i dr.), u čijem razvoju etiološku ulogu imaju hemolitički streptokok grupe A, kao i zarazne bolesti (edematozna bolest prasadi, erizipela itd.).
Patogeneza Promene u oticanju sluzokože sastoje se u kršenju sinteze međućelijske supstance ili u njenom površinskom razgradnji pod dejstvom hijaluronidaze egzogenog (hemolitički streptokok i dr.) ili endogenog porekla, kao iu uslovima sve veće hipoksije tkiva sa razvojem ekološke acidoze. To dovodi do depolimerizacije proteinsko-polisaharidnog kompleksa i nakupljanja oslobođenih kiselih glikozaminoglikana (posebno hijaluronske i hondroitinsulfurne kiseline), koji, imaju hidrofilna svojstva, uzrokuju povećanje permeabilnosti tkiva i krvnih žila, edem seroznog tkiva sa impregnacijom proteina plazme. albumini, globulini i glikoproteini).
Mikroskopski mukoidno oticanje vezivnog tkiva određeno je bazofilijom i metahromazijom vlakana i mljevene tvari (na primjer, toluidin plavo boji kisele glikozaminoglikane crveno, pikrofuksin - ne crveno, već žuto-narandžasto). Suština metahromazije (od grčkog meta - promjena, chromasia - bojenje) je sposobnost glikozaminoglikana da izazovu polimerizaciju boje. A ako boja kao monomer ima plavu boju, kao dimer, trimer je ljubičasta, onda je kao polimer crvena (tautomerizam). Promjene u molekularnoj strukturi kolagenih vlakana praćene su njihovim oticanjem, neravnomjerno izraženim povećanjem volumena i zamućenjem kontura i strukture, defibracijom, a promjena intersticijalne tvari je praćena nakupljanjem T-limfocita i histiocita.
Makroskopski organ ostaje nepromijenjen, ali su mišićno-koštane i barijerne funkcije vezivnog tkiva narušene.
Exodus. Moguća je potpuna obnova oštećenih struktura ili prijelaz u fibrinoidno oticanje.
fibrinoidno oticanje- duboka dezorganizacija vezivnog tkiva strome organa, žila, koju karakterizira pojačana depolimerizacija proteinsko-polisaharidnih kompleksa osnovne tvari i fibrilarnih struktura s naglim povećanjem propusnosti vaskularnog tkiva. U vezi sa plazmoragijom, vezivno tkivo je impregnirano proteinima krvi (albumin, globulini, glikoproteini, fibrinogen). Kao rezultat precipitacije ili kemijske interakcije ovih spojeva nastaje kemijski složena heterogena tvar - fibrinoid, koja uključuje proteine i polisaharide raspadajućih kolagenih vlakana, glavnu tvar i krvnu plazmu, kao i stanične nukleoproteine.
razlozi: isti alergijski, infektivni faktori, neurotrofični poremećaji koji uzrokuju oticanje sluzokože, ali djeluju sa većom snagom ili trajanjem. Kao lokalni proces, fibrinoidno oticanje se opaža u žarištima kronične upale.
Patogeneza. Fibrinoidne promjene, kao naknadna faza mukoidnog oticanja, nastaju ako se produbi proces dezorganizacije vezivnog tkiva, dođe do raspada ne samo glavne supstance, već i kolagena i drugih fibrilarnih struktura, depolimerizacije glikozaminoglikana, raspadanja kolagenih vlakana i njihova impregnacija proteinima plazme, uključujući i grubi protein - fibrinogen, koji je obavezna komponenta fibrinoida. Istovremeno je poremećena fibrilogeneza, posebno biosinteza kiselih glikozaminoglikana u mezenhimskim ćelijama, a primećuje se i proliferacija T-limfocita i histiocita. Hemijska interakcija i polimerizacija produkata razgradnje osnovne supstance, kolagena i proteina plazme, praćeni su stvaranjem neobičnih proteinsko-polisaharidnih fibrinoidnih kompleksa.
Histološke promjene javljaju se u dvije faze: fibrinoidno oticanje i fibrinoidna nekroza. Kod fibrinoidnog oticanja bilježi se dezintegracija osnovne tvari, oticanje i djelomična dezintegracija kolagenih i elastičnih vlakana, plazmoragija s impregnacijom vezivnog tkiva albuminima, plazma globulinima i fibrinogenom, što se otkriva histohemijskim i imunofluorescentnim metodama. Kolagen, formirajući guste netopive spojeve s fibrinogenom i drugim tvarima, mijenja svoja tinktorijalna svojstva: postaje eozin-, pironino- i argirofilan, pikrofuchsin postaje žut, reakcija PAS je oštro pozitivna. Proces se završava potpunim uništenjem vezivnog tkiva uz razvoj fibrinoidne nekroze. U ovom slučaju, tkivo ima oblik zrnasto-grudaste ili amorfne mase, koja uključuje produkte razgradnje kolagenih vlakana, glavne tvari i proteina plazme. Sa potpunom depolimerizacijom slobodnih glikozaminoglikana, metahromazija obično nije izražena. Oko nekrotičnih masa se razvija produktivna upala sa formiranjem nespecifičnih granuloma koji se sastoje od T-limfocita i makrofaga.
Makroskopski fibrinoidne promjene u vezivnom tkivu su jedva primjetne, nalaze se pod mikroskopom.
Klinički značaj fibrinoidno oticanje je rezultat kršenja ili isključivanja funkcije zahvaćenog organa.
Exodus povezan sa tokom osnovne bolesti u kojoj se ovaj proces razvija. Fibrinoidne mase se mogu resorbirati, zamijeniti vezivnim tkivom, koje podliježe sklerozi ili hijalinozi.
Hialinoza(od grčkog hyalos - providan, staklast), ili hijalinska distrofija, - vrsta fizičko-hemijske transformacije vezivnog tkiva u vezi sa formiranjem kompleksnog proteina - hijalina, sličnog morfološkim karakteristikama glavnoj supstanci hrskavice. Hijalin daje tkivima posebno fizičko stanje: postaju homogena, prozirna i gušća. Sastav hijalina uključuje glikozaminoglikane i proteine vezivnog tkiva, krvnu plazmu (albumini, globulini, fibrinogen), kao i lipide, kalcijeve soli. Podaci elektronske mikroskopije sugeriraju da hijalin sadrži vrstu fibrilarnog proteina (fibrin). Hijalin je otporan na djelovanje kiselina, lužina, enzima, intenzivno obojen kiselim bojama (eozin, kiseli fuksin ili pikrofuchsin) u crvenu ili žutu, daje PAS-pozitivnu reakciju.
Razlozi. Hialinoza se razvija kao rezultat različitih patoloških procesa: impregnacije plazmom, mukoidnog i fibrinoidnog oticanja vezivnog tkiva. Fiziološki prototip hijalinoze je starenje.
Sistemska hijalozažila i vezivnog tkiva uočava se kod bolesti kolagena, arterioskleroze, infektivnih i toksičnih bolesti, kroničnih upala, bolesti povezanih s poremećenim metabolizmom proteina, posebno kod visokoproduktivnih krava i svinja. Izražena hialinoza krvnih žila javlja se kod kroničnog glomerulonefritisa, posebno kod pasa. Uz to se javlja i lokalna hialinoza (skleroza) u novoformiranom vezivnom (ožiljkom) tkivu.
Patogeneza. Važnu ulogu u nastanku i razvoju sistemske hijalinoze imaju hipoksija tkiva, oštećenje endotela i bazalnog sloja vaskularnog zida, poremećaji u sintezi i strukturi retikularnih, kolagenih, elastičnih vlakana i glavne supstance vezivnog tkiva. tkiva. U ovom slučaju dolazi do povećanja vaskularne i tkivne propusnosti, impregnacije tkiva proteinima plazme, njihove adsorpcije s stvaranjem složenih proteinskih spojeva, taloženja i zbijanja proteinskih masa.
Imunološki mehanizmi su takođe uključeni u nastanak hijalinoze, jer je dokazano da hijalinske mase imaju neka svojstva imunokompleksa antigen-antitelo.
Histološki hijalin se nalazi u međućelijskoj supstanci vezivnog tkiva. Sistemska hijaloza zidova krvnih sudova i vezivnog tkiva manifestuje se stvaranjem hijalina u glavnoj supstanci intime i perivaskularnog vezivnog tkiva arterija i kapilara. Na kraju se formira homogena gusta proteinska masa obojena kiselim bojama. Iako je hijalin indiferentna tvar, njegovo nakupljanje je praćeno zadebljanjem stijenke žile, pomicanjem medija hijalinom masom sa sužavanjem lumena, do potpunog zatvaranja (obliteracije) u malim žilama. Nekrotizacija tkiva koja su podvrgnuta hijalinozi može biti praćena njihovom kalcifikacijom, rupturama zida žila sa pojavom krvarenja i tromboze. U žljezdanim organima, hialinoza vezivnog tkiva praćena je zadebljanjem bazalnih membrana žlijezda, kompresijom žljezdanog epitela, nakon čega slijedi njegova atrofija. Lokalna hijalinoza se javlja u žarištima hronične upale, u novonastalom vezivnom tkivu (kapsule vezivnog tkiva i stari ožiljci). Istovremeno, kolagena vlakna bubre, spajaju se u homogena tkiva, a ćelije atrofiraju.
Makroskopski organi i tkiva zahvaćeni hijalinozom u slabom stepenu nemaju izrazito izražene promjene, proces se otkriva samo pod mikroskopom. Uz izraženu hijalinozu, žile gube elastičnost, a zahvaćeni organi postaju blijedi i gusti. Kada se kalcijeve soli precipitiraju u hijalinske mase, one se još više zbijaju.
Funkcionalna vrijednost hijalinoza zavisi od njenog stepena i prevalencije. Sistemska hialinoza uzrokuje disfunkciju organa, posebno njihovih krvnih žila, uz razvoj atrofije, rupture i druge ozbiljne posljedice. Lokalna hialinoza možda neće uzrokovati značajne funkcionalne promjene.
Exodus drugačije. Utvrđeno je da se hijalinske mase mogu olabaviti i otopiti ili mucirati, na primjer, u ožiljcima, u tzv. keloidima. Međutim, u većini slučajeva, rasprostranjena hialinoza se manifestira kao nepovratan proces.
Diferencijalna dijagnoza. Patološku hialinozu treba razlikovati od fiziološke, koja se očituje u procesu involucije i normalnog starenja tkiva (na primjer, involucija žutog tijela, žila maternice, mliječne žlijezde itd.). Istovremeno, hialinoza maternice i mliječne žlijezde je reverzibilna zbog povećane funkcije organa. Izvana, hijalinska transformacija mrtvih tkiva, produkata izlučivanja slična je hijalinozi (na primjer, formiranje hijalinskih cilindara kod nefroze-nefritisa, hijalinskih tromba, fibrinske hijalinizacije itd.).
Amiloidoza (amiloidna degeneracija) karakterizira patološka sinteza posebnog fibrilarnog proteina (preamiloida) u stanicama retikuloendotelnog sistema, nakon čega slijedi formiranje amiloida, kompleksnog glikoproteina. R. Virchow (1859) je ovaj glikoprotein uzeo za jedinjenje nalik škrobu (amilum - škrob) zbog njegovog karakterističnog bojenja u plavo sa jodom i sumpornom kiselinom. Zbog snage hemijskih veza, amiloid je otporan na kiseline, lužine, enzime i otporan je na propadanje. Kiseli glikozaminoglikani (hondroitin sulfat) s različitim stupnjevima polimerizacije daju amiloidu svojstvo metahromazije, što ga razlikuje od hijalina i drugih proteina. Amiloid mrlje ružičasto-crveno sa encijan i kresil ljubičastom na ljubičastoj pozadini tkiva. Jodgrun također boji amiloidnu crvenu boju, a Kongo crvena mrlja smeđe smeđu. Kongo crveno, uneseno u krv, može se akumulirati u amiloidnoj masi in vivo, koja se koristi za doživotnu dijagnozu amiloidoze. Amiloidne mase daju PAS-pozitivnu reakciju. Hemijski sastav amiloida može biti različit. S tim u vezi ispadaju neke šarene amiloidne reakcije (na primjer, metahromazija) (paramiloid).
Uzroci sistemske amiloidoze: upalni, gnojni, nekrotični procesi bilo kojeg porijekla i intoksikacija. U tim slučajevima, amiloidoza se razvija kao komplikacija bolesti (sekundarna ili tipična amiloidoza) uzrokovana razgradnjom proteina tkiva (na primjer, kod tuberkuloze, malignih tumora, nespecifičnih upalnih procesa sa supuracijom itd.). Sekundarna amiloidoza se uočava kod visokoproduktivnih krava u laktaciji, ptica, krznenih životinja, konja („pelutna bolest“) itd. Uzroci atipične primarne (idiopatske) i senilne amiloidoze karakteristične za ljude nisu poznati. Genetska amiloidoza je nasljedna enzimopatija ili anomalija (mutacija) u genetskom aparatu RES ćelija. U eksperimentu na laboratorijskim životinjama, amiloidoza se može izazvati parenteralnom primjenom stranog proteina (kazeina), kao i stvaranjem žarišta kroničnog gnojenja. Zbog produžene parenteralne primjene stranog proteina, amiloidoza se razvija kod konja koji proizvode imune serume.
Uzroci lokalne amiloidoze: kronični upalni procesi sa stagnacijom krvi i limfe.
Patogeneza amiloidoza je kompleksna.
Prema teoriji disproteinoze(K. Apitz, E. Randerath, 1947) amiloid nastaje na osnovu poremećene sinteze proteina sa pojavom paraproteina ili paraglobulina u krvi i razvojem disproteinemije i hipergama globulinemije. Ovi proizvodi grube proteinske frakcije krvne plazme, koji se oslobađaju kroz endotelnu barijeru, prvenstveno u slezeni, jetri i bubrezima, spajaju se sa kiselim glikozaminoglikanima, koji se oslobađaju pod uticajem proteina plazme i tkivnih hijaluronidaza, i formiraju amiloid.
Prema teoriji autoimunosti(Loeschke, Letterer, 1962) izmijenjena reaktivnost organizma i autoimuni procesi su od presudnog značaja u stvaranju amiloida. U mnogim procesima kompliciranim amiloidozom akumuliraju se proizvodi raspadanja tkiva, leukociti i bakterije s antigenskim svojstvima. Moguće je da poremećaji u reakcijama u imunološkom sistemu povezani s viškom antigena i nedostatkom antitijela dovode do pojave precipitina specifičnih za tkivne proteine u krvi i fiksacije proteinskog kompleksa na mjestima stvaranja antitijela (Letterer) . Ova teorija je zadržala svoj značaj za eksperimentalnu i sekundarnu amiloidozu. Ona ne objašnjava mehanizam razvoja idiopatske, genetske i senilne amiloidoze.
Teorija stanične lokalne geneze(G. Teilum, 1962) smatra amiloid proizvodom sinteze proteina ćelijama mezenhimskog sistema sa izopačenim metabolizmom („mezenhimska bolest“). To potvrđuje selektivnost oštećenja ovog sistema i intracelularno formiranje preamiloidnih fibrila od strane ćelija mezenhimske prirode.
Novi mutaciona teorija amiloidoze(E. Benditt, N. Eriksen, 1977; V. V. Serov, I. A. Šamov, 1977), koji može postati univerzalan za razumijevanje patogeneze svih njegovih poznatih oblika sa
uzimajući u obzir raznolikost faktora koji uzrokuju mutaciju. Prema ovoj teoriji, imunokompetentni sistem ne prepoznaje mutirane ćelije i ne eliminiše se, budući da su amiloidni fibrili izuzetno slabi antigeni. Nastala reakcija resorpcije amiloida (amiloidoklazija) na samom početku njenog formiranja je nedovoljna i brzo se potiskuje. Postoji imunološka tolerancija (tolerancija) organizma na amiloid i ireverzibilni razvoj amiloidoze. Teorija mutacije objašnjava blizinu amiloidoze tumorskim procesima.
Histološke i makroskopske promjene ovise o uzroku nastanka, odnosu prema različitim stanicama vezivnog tkiva i lokalizaciji amiloida.
U tipičnoj općoj amiloidozi, najčešće kod domaćih životinja, amiloid ispada duž retikularnih vlakana vaskularnih i žljezdanih membrana i u periretikularne prostore parenhimskih organa (periretikularna ili parenhimska amiloidoza). Zahvaćeni su jetra, slezena, bubrezi, rjeđe nadbubrežne žlijezde, hipofiza, vlastita membrana crijevnih žlijezda, intima kapilara i arteriola. Preamiloidna fibrila se akumuliraju u ćelijama vezivnog tkiva, nestaju ribozomi, hipertrofija mitohondrija (gigantske mitohondrije) i Golgijevog lamelarnog kompleksa (A. Polikar, M. Bessey, 1970).
Akumulacija amiloida u tkivu je praćena atrofijom i smrću parenhimskih elemenata organa.
Amiloidoza jetre karakteriše formiranje amiloida oko sinusoidnog prostora (prostora Disse) između zvezdastih retikuloendoteliocita i ćelija jetre (slika 8). Amiloid se također nalazi u zidovima interlobularnih kapilara i arteriola. Kako se amiloidna tvar akumulira, jetra se povećava u veličini, poprima blijedosmeđu boju, gušću, a kod konja mlohavu konzistenciju. Kod konja može dostići masu od 16-33 kg, dok oko 10% slučajeva završava rupturom jetre usled topljenja strome (A.P. Gindin, 1959), pojavljuju se modrice koje se često završavaju fatalnim krvarenjem u trbušnoj duplji.
Amiloidoza slezene manifestira se u dva oblika: folikularnom i difuznom. U prvom slučaju, amiloid se taloži u retikularnom tkivu folikula, počevši od njihove periferije. Retikularno i limfoidno tkivo folikula atrofiraju i zamjenjuju ih amiloidne mase. Makroskopski amiloidno izmijenjeni folikuli na rezu izgledaju kao prozirna zrna koja podsjećaju na zrna kuhanog saga („sago slezena“). U drugom slučaju, amiloid se taloži manje-više ravnomjerno kroz cijelu retikularnu stromu organa i ispod endotela sinusa. Kod difuzne amiloidoze, slezena je povećana u veličini, guste konzistencije, a kod konja je žilava; površina reza je glatka, svijetlo crveno-braon, podsjeća na sirovu šunku ("masna" ili "šunka" slezena). Kod konja je moguća ruptura organa i krvarenja.
u bubrezima amiloid se taloži prvenstveno u mezangu i iza endotela kapilarnih petlji i glomerularnih arteriola, kao i u retikularnoj stromi kortikala i medule, u zidovima arteriola i malih arterija, rjeđe u bazalnom sloju ispod epitela tubule. Bubrežni glomeruli postupno atrofiraju, epitel tubula, osim toga, prolazi kroz granularnu i hijalinsku degeneraciju. Kako se amiloid nakuplja, bubrezi se povećavaju u veličini, postaju blijedosmeđi, voštani i suhi. Uz izoliranu leziju bubrežnih glomerula, izgledaju kao sivkasto-crvene mrlje.
U drugim organima(nadbubrežne žlijezde, hipofiza, crijeva) amiloid se taloži u retikularnoj stromi i bazalnom sloju krvnih žila i žlijezda. Zbog činjenice da organi sa amiloidozom dobijaju voštani ili masni izgled, mađarski patolog K. Rokitansky je 1844. godine opisao ove promene pod nazivom bolest lojnica.
Primarna atipična amiloidoza sa sistemskim oštećenjem adventicije krvnih sudova srednjeg i velikog kalibra, miokarda, prugastih i glatkih mišića, gastrointestinalnog trakta, pluća, nerava, kože kod domaćih životinja - relativno rijedak "" fenomen. Zapažen je kod bolesti vezivnog tkiva infektivno-alergijskog porijekla (reumatizam i dr.), virusna plazmocitoza itd. U ovom slučaju amiloid se nalazi uglavnom u zidovima kapilara i arterija, u plazma membranama fibroblasta i kolagenim vlaknima (perikolagena amiloidoza). ne daje uvijek reakciju metahromazije (paramiloid) i pokazuje tendenciju razvoja ćelijske proliferativne reakcije sa stvaranjem nodularnih izraslina.
Rijetke atipične oblike amiloidoze uključuju lokalna amiloidoza sa taloženjem amiloidnih masa u vezivnom tkivu i zidu krvnih sudova u izolovanom delu organa. Nalazi se u plućnim alveolama kod hronične pneumonije, u sluzokoži nosne duplje kod konja, u prostati kod starih životinja (psa i dr.), u centralnom nervnom sistemu na mestu distrofno izmenjenih i mrtvih nervnih ćelija, kao iu sluzokoži drugih organa.
Funkcionalna vrijednost amiloidoza je povezana s razvojem atrofije i odumiranja parenhimskih stanica i progresivnim zatajenjem organa (jetrene, bubrežne), poremećajima cirkulacije krvi i limfe i mogućnošću rupture organa (posebno kod konja), ponekad praćeno fatalnim krvarenjem.
Exodus opća amiloidoza je obično nepovoljna. Međutim, postoje eksperimentalni, klinički i patomorfološki podaci da se amiloidne mase mogu apsorbirati uz sudjelovanje gigantskih stanica, ako se eliminira uzrok njegovog nastanka (M. N. Nikiforov, A. I. Strukov, B. I. Migunov, 1971). Kod životinja, amiloidoza je jedan od ireverzibilnih procesa.
Hematini su oksidativni oblik hema. Imaju oblik anizotropnih zrnaca ili tamno smeđih kristala, sadrže željezo u vezanom obliku, obezboje se vodikovim peroksidom, otapaju se u lužinama i slabo su topljivi u kiselinama. Tu spadaju pigmenti: malarija (hemomelanin), hlorovodonična kiselina (hemin) i formalin. Zbog stvaranja velike količine krvnih pigmenata, slezena, koštana srž i jetra mogu dobiti škriljasto sivu boju. Hematin hidrohlorid nastaje djelovanjem želučanih enzima i hlorovodonične kiseline na hemoglobin, dajući erozije i čireve želuca, kao i njegov sadržaj u prisustvu krvarenja, smeđe-crne boje. Formalinski pigment se nalazi u tkivima bogatim krvlju kada su fiksirani u kiselom formalinu. Taloži se u obliku zrnaca, grudica ili tankih tamnosmeđih kristala. Pigment nestaje nakon što se histosekcija tretira slabom (1-2%) vodenom ili alkoholnom (50-70%) otopinom kaustične alkalije (KOH).
Porfirini- prekursori hema, bez gvožđa. Njihovo prekomjerno nakupljanje u krvi (porfirinemija) praćeno je razvojem hemolitičke anemije i splenomegalije, smeđe-žute ili gotovo crne pigmentacije bubrega (porfirinurija uz prisustvo crvene mokraće), skeleta (osteohemohromatoza) i dentina zuba. kod svinja i goveda. Pigmentna zrna se luče u ćelijama mononuklearno-makrofagnog sistema koštane srži i u epitelu mokraćnih tubula bubrega, dajući im radijalnu prugastost. Razvoj kongenitalne (idiopatske) porfirije povezan je sa blokiranjem u eritrocitima enzimske konverzije protoporfirina III u uroporfirin III, koji je u osnovi strukture hema. Stečena porfirija se javlja kod trovanja (olovo, barbiturati i dr.), hipovitaminoze (pelagra), perniciozne anemije i nekih oboljenja jetre. Naslage porfirina u koži izazivaju fotodinamički efekat (eritem, dermatitis).
pigment gvožđa Takođe nastaje tokom razgradnje mioglobina. Miosiderin se nalazi u atrofiranju mišićnog tkiva, ali u većoj mjeri u njegovoj distrofiji i voštanoj nekrozi povezanoj s bolešću bijelih mišića životinja, paralitičnom mioglobinurijom konja. Istovremeno, mioglobinemiju prati razvoj miogemosideroze organa bogatih retikuloendotelnim tkivom (slezena, jetra, limfni čvorovi itd.), oslobađanje otopljenog pigmenta u urinu (mioglobinurija sa crvenim urinom) i njegovo taloženje u epitelnih ćelija urinarnih tubula.
Kod nekih trovanja (nitriti i dr.) opća pigmentacija je povezana sa stvaranjem methemoglobina (svijetlosmeđa boja krvi). Hemoglobin može postati zelenkast ili crn kada se kombinuje sa vodonik sulfidom i formira željezo sulfid (lažna melanoza). Kod svježih leševa konja pigmentacija se uočava u ileumu kao ravne ili uzdignute crne površine.
Proteinogeni (tirozin-triptofan) pigmenti uključuju melanin, andrenohrome i pigment enterohromafinskih ćelija.
Melanin(od grčkog melanos - crn) nastaje u melanoblastima - ćelijama neurogene prirode bazalnog sloja epidermisa, folikula dlake, retine i šarenice, dajući im specifičnu boju (crna, smeđa, žuta, crvena). Proizvod je prirodne polimerizacije tirozina i triptofana, koji se u prisustvu vitamina C sintetiše u bezbojni promelanin, a pod uticajem tirozinaze (dopaoksidaze) prelazi u melanin. Pigment ne sadrži gvožđe i mast, obezbojava vodonik peroksidom i drugim jakim oksidantima, redukuje rastvor amonijaka srebrnog nitrata u metalno srebro, rastvorljivo samo u alkalijama. U citoplazmi melanoblasta pigment se taloži u obliku zrnaca i grudica tamno smeđe boje. Migraciju melanina u tijelu osiguravaju makrofagi - melanofori, koji zbog nedostatka tirozinaze nisu sposobni za sintezu melanina. Za razliku od melanoblasta, oni ne daju pozitivnu dopa reakciju.
Povrede melanogeneze manifestiraju se povećanim stvaranjem melanina, njegovim nakupljanjem na neuobičajenim mjestima, nestankom ili odsutnošću pigmenta. Sva tri tipa metaboličkih poremećaja mogu biti stečena ili kongenitalna i biti rasprostranjena ili lokalna.
Prekomjerno stvaranje melanina u koži i njegovo taloženje u unutrašnjim organima naziva se opšta melanoza, koja se javlja uglavnom kod goveda i sitne goveda, posebno kod teladi i ovaca. Priroda melanoze je nepoznata, ali se vjeruje da je ovaj proces porijeklom iz hrane. Primjećuje se kod životinja koje pasu na pašnjacima sa zatopljenim i zakiseljenim tlima. Melanin se taloži u jetri, plućima (slika 9) i na seroznom integumentu, rjeđe u membranama mozga i kičmene moždine, koje poprimaju tamno smeđu ili smeđe-crnu boju. Obično se melanoza otkriva nakon klanja životinja. Rasprostranjena melanoza s pigmentacijom kože i oralne sluznice u bronzanoj boji uočena je kod pasa s Addisonovom bolešću zbog oštećenja nadbubrežne žlijezde. Povećana pigmentacija kože javlja se kod domaćih životinja s kroničnim bolestima praćenim iscrpljenošću.
Lokalizirana prekomjerna pigmentacija koža je povezana sa benignom ili malignom proliferacijom melanoblasta sa stvaranjem melanoma. Često se javljaju kod sivih konja i pasa. Izvori njihovog pojavljivanja su madeži (naevus).
Kao rezultat raspadanja pigmentiranih tumora može se razviti sekundarna opća melanoza.
Kongenitalno nedovoljno stvaranje melanina ili njegovo potpuno odsustvo u tijelu naziva se albinizam (albus - bijeli). Ovaj fenomen je povezan sa recesivnim genom i odsustvom tirozinaza koje stvaraju pigment. Uočava se kod sivih konja, kod goveda nekih rasa (herefordi), ovaca, krznaša, polarnih medvjeda, zečeva itd. Često se javljaju i drugi genetski defekti (npr. patološke granule u leukocitima), kao i opća slabost. i podložnost bolestima. Ova bolest kod ljudi i životinja opisana je kao Shediak-Higashi sindrom. Može doći do lokalne kongenitalne depigmentacije kože (vitiligo). Stečene nepigmentirane mrlje, nazvane leukoderma (od grčkog leukos - bijeli, derma - koža), nastaju nakon dugotrajne upale i drugih kožnih lezija (rane, čirevi, kod slučajnog oboljevanja konja i sl.).
Na lipidogene pigmente, odnosno lipopigmente pripadaju lipofuscinu, ceroidu i lipohromima. Sadrže masne i proteinske supstance.
Lipofuscin- glikolipoprotein, nastaje u ćelijama u procesu autooksidacije fosfolipida. Pod mikroskopom izgleda kao zrna i grudvice smeđe boje. Pigment je sudanofilan, obojen crvenom grimizom, nerastvorljiv u organskim otapalima i kiselinama, djelomično rastvorljiv u alkalijama, za razliku od melanina, ne crni u interakciji sa srebrnim nitritom. Lipofuscin je normalna ćelijska komponenta uključena u oksidativne procese.
Patološka pigmentacija lipofuscinom, posebno jetre, bubrega, srčanih i skeletnih mišića, nervnih ćelija, uočava se kod iscrpljujućih bolesti, na primjer, kod nedostatka ugljikohidrata-proteina kod krava visoke produktivnosti, s atrofijom parenhimskih organa, uključujući i starije životne dobi. (senilna atrofija). Makroskopski, kako se pigment nakuplja, organ dobija smeđu boju (smeđa atrofija).
Pigmenti hemofuscin, koji se nalaze u jetri konja sa infektivnim encefalomijelitisom, i ceroid, čije je stvaranje povezano sa hipovitaminozom E, po fizičko-hemijskim i biološkim svojstvima identični su lipofuscinu.
Lipohromi- pigmenti koji daju žutu boju masnom tkivu, kori nadbubrežne žlijezde, žumancetu, krvnom serumu itd. U lipohrome spada i lutein, pigment žutog tijela jajnika. To su lipidi u kojima su otopljeni obojeni ugljovodonici - karotenoidi i flavini. Njihovo stvaranje usko je povezano s metabolizmom proteina i masti i razmjenom biljnih pigmenata. Kada se tretiraju kiselinama (na primjer, sumpornom), potonje daju nestabilnu zelenkasto-plavu boju, blijede pod utjecajem oksidativnih enzima, imaju zelenu fluorescenciju na ultraljubičastom svjetlu i talože se u kristale pod utjecajem alkohola. Pojačana pigmentacija s lipohromima masnog tkiva je zabilježena s osiromašenjem zbog kondenzacije pigmenta. U tom slučaju, vlakno poprima jarko žutu boju. Žuta mrlja i žuto-smeđa boja kostiju nalaze se kod poremećaja metabolizma lipida i vitamina (dijabetes melitus i dr.), kao i na mjestima nakupljanja holesterola (u ateromatoznim plakovima i ksantomima).
Egzogena pigmentacija povezana sa ulaskom u organizam stranih boja iz spoljašnje sredine. Najčešće je taloženje u plućima čestica prašine mineralnog, biljnog ili životinjskog porijekla uz razvoj pneumokonioze (od grčkog peutop - pluća, conia - prašina). Ove čestice se adsorbuju na sluznicama, prodiru u epitelne ćelije, fagocitiraju ih makrofagi, prodiru u limfne sudove i čvorove, a mogu se uneti i u druge organe.
Među ovim bolestima, antrakoza pluća povezana s taloženjem ugljene prašine u njima je od velike praktične važnosti. Antrakoza je najčešća kod konja i pasa. Pluća u isto vrijeme dobivaju difuznu ili šarenu škriljasto-crnu ili škriljevastu boju. Značajno taloženje ugljene prašine uzrokuje upalne promjene, razvoj vezivnog tkiva i induraciju pluća. Iz pluća se čestice uglja šire u regionalne limfne čvorove, rjeđe u slezenu i jetru. Antrakoza mezenteričnih limfnih čvorova često se javlja kod goveda kada se životinje hrane prašnjavom hranom. Taloženje u plućima silicijum dioksida, glinice, grudica kvarca sa stvaranjem bijelih žarišta naziva se silikoza.
Uz produženo liječenje životinja preparatima srebra, može se razviti artroza. Soli srebra se talože u epitelu urinarnih tubula i u mezangumu vaskularnih glomerula, kao iu retikuloendotelnim ćelijama jetre i drugih organa, čija tkiva dobijaju sivu (čeličnu) boju. Neke ljekovite (na primjer, metilensko plavo, pikrinska kiselina) i boje koje se koriste u tetovažama životinja daju organima određenu boju.
Kršenje razmjene nukleoproteina. Nukleoproteini su spojevi proteina sa nukleinskim kiselinama - deoksiribonukleinskom (DNK) i ribonukleinskom (RNA). Poremećaji metabolizma nukleoproteina uključuju dijatezu mokraćne kiseline i infarkt mokraćne kiseline.
Dijateza mokraćne kiseline(od grčkog dijateza - predispozicija) karakterizira pojačano stvaranje i nakupljanje mokraćne kiseline i njenih soli u krvi (hiperuremija), praćeno taloženjem kristala mokraćne kiseline i amorfnog natrijum urata u različitim tkivima i organima. Najčešće se dijateza mokraćne kiseline javlja kod ptica, posebno iz reda pilića, rjeđe kod sisara (psa i dr.).
Pojava ove bolesti kod ptica u kavezima, uključujući i divlje ptice u zoološkom vrtu, povezana je sa obilnom i dugotrajnom ishranom proteinima životinjskih proizvoda (meso, riba, meso i kosti i riblje brašno) i biljnog (koncentrovana hrana) porekla, posebno u nedostatku zelene i druge vitaminske hrane (posebno vitamina A). Od unutrašnjih faktora tome doprinose bolesti bubrega i jetre.
Lokalizacija patoloških procesa u određenim organima može se objasniti posebnim fizičko-hemijskim i alergijskim stanjem tkiva koje zadržavaju mokraćnu kiselinu i njene soli.
Mikroskopskim pregledom na mjestima taloženja mase sa blistavim kristalima mokraćne kiseline i amorfnim sedimentima njenih soli otkrivaju se nekrotična žarišta, oko kojih se formira upalni infiltrat uz prisustvo leukocita, histiocita, a posebno karakterističnih gigantskih stanica. Nakon eksudativno-ćelijske reakcije nastaju manje ili više izražene proliferativne promjene koje su praćene stvaranjem granulacijskog i fibroznog tkiva uz deformaciju zahvaćenih organa.
Makroskopske promene karakteriše činjenica da se mokraćna kiselina i natrijum urat talože na seroznim membranama, u bubrezima i drugim unutrašnjim organima, kao i u zglobovima ekstremiteta (hrskavica, sinovija, ovojnice tetiva). Stoga postoje visceralni, zglobni i mješoviti oblici bolesti.
Sa visceralnom dijatezom mokraćne kiseline(nalazi se samo kod ptica) mokraćna kiselina i njene soli u obliku belih kredastih masa ili finog kristalnog praha se talože na seroznim membranama trbušne duplje, vazdušnim kesama, bubrezima, jetri, slezeni, crevima, srcu i plućima, kao i kao i drugi organi. Ispod navlaka koje se lako skidaju otkriva se upaljeni serozni omotač. U teškom obliku dijateze, slojevi postaju gipsani, serozne membrane se lijepe i rastu zajedno. U unutrašnjim organima, posebno u bubrezima, kao i u jetri, pankreasu, srčanim i skeletnim mišićima (mišići nogu, krila), u endokardu i endotelu velikih krvnih sudova, ispod kože, u žlezdanom želucu, naslage mokraćne kiseline i urata nalaze se u obliku razbacanih tačaka, mrlja, pruga ili bijelo-žutih čvorića sklonih spajanju. U tom slučaju se zahvaćeni organi, posebno bubrezi, povećavaju u volumenu.
Zglobni oblik bolesti ili giht(od grčkog pous - noga, agrios - tvrd), karakteriziran taloženjem mokraćne kiseline i urata na sinovijalnim membranama zglobova i ovojnica tetiva, u kapsulama zglobova i njihovim okolnim tkivima. Najčešće su zahvaćeni zglobovi skočnog zgloba i nožnih prstiju. Zahvaćeni zglobovi su uvećani, tvrdi, deformisani, sa srednje gustim fibroznim čvorovima - gihtnim kvržima (tophi unci), u kojima se nalazi suha, kredasta ili kremasta masa. Istovremeno u zglobnoj hrskavici mogu nastati nekroze i ulceracije u vidu zareza (usura), a oko njih dolazi do upalne reakcije sa nakupljanjem divovskih stanica i rastom vezivnog tkiva.
Infarkt bubrega mokraćne kiseline(infarcire - nadjev, nadjev) nalaze se uglavnom kod novorođenčadi. Mokraćna kiselina i njene soli se talože u homogenu glikoproteinsku masu u lumenu rektalnih tubula, u apikalnom dijelu žljezdanog epitela i u stromi organa, u meduli i papilama bubrega, formirajući bjelkaste, bjelkaste boje. žućkasta ili crvenkasto-žuta radijalno raspoređena zrna, grudvice, granule ili pruge.
U lumenu direktnih tubula i u proksimalnom nefronu nalaze se u manjem broju.
Srčani udari mokraćne kiseline nastaju u vezi sa masivnim propadanjem eritrocita sa jezgrom pri prelasku fetusa na način vanjskog disanja, uz restrukturiranje ishrane i metabolizma. Istovremeno, koncentracija mokraćne kiseline u krvi naglo raste. Nastanak srčanog udara, osim toga, doprinosi gubitku vode novorođenčeta. Kao što su naša zapažanja pokazala, konglomerati kristala amonijeve mokraćne kiseline i labava proteinska masa koja ih veže mogu biti osnova za razvoj urolitijaze kod mladih životinja, posebno kuna.
Intarzija mrtvih masa. Kod odraslih životinja, mokraćna kiselina i njene soli mogu zasićiti mrtva tkiva i taložiti se u njima. Ovo se dešava u tkivima mokraćnih kanala kada mrtva masa dođe u kontakt sa urinom.
poremećaji metabolizma nukleoproteina. Kod dijateze mokraćne kiseline poremećene su funkcije zahvaćenih organa (bubrezi, jetra itd.). Zglobni oblik bolesti je praćen deformitetom, slabom pokretljivošću i bolnošću zahvaćenih zglobova. Hiperuremija i hiperazotemija mogu uzrokovati iznenadnu smrt životinje. Naslage mokraćne kiseline i urata u organima uzrokuju ireverzibilne (nekrotične) promjene u zahvaćenim tkivima.
Poremećaji metabolizma glikoproteina. Glikoproteini su kompleksna jedinjenja proteina sa polisaharidima koji sadrže heksoze, heksozamine i heksuronske kiseline. To uključuje mucine i mukoide (za druge glikoproteine, pogledajte "Distrofije ugljikohidrata").
Mucini čine osnovu sluzi koju luči epitel sluzokože i žlijezda. Sluz ima izgled prozirne viskozne tvari koja pod utjecajem slabe octene kiseline ili alkohola ispada u obliku tanke vlaknaste mreže. Sastav sluzi uključuje neutralne ili kisele polisaharide - proteinske komplekse koji sadrže hijaluronsku i hondroitin sumpornu kiselinu (glikozaminoglikane), koji sluzi daju hromotropna ili metahromatska svojstva. Thionin i kresil ljubičasta sluz postaju crvena, a tkiva plava ili ljubičasta. Mucikarmin mu daje crvenu boju, a toluidin plavu - lila-ružičastu.
Formiranje sluzi kao patološki proces ima zaštitnu i adaptivnu vrijednost. Mucin štiti sluznicu od fizičkog oštećenja i iritacije od kemikalija. Sluz je nosilac probavnih enzima.
Mukoidi ili supstance slične sluzi („pseudomucini“) nisu homogena hemijska jedinjenja koja sadrže proteine i glikozaminoglikane. Oni su dio različitih tkiva: kosti, hrskavice, tetive, srčani zalisci, zidovi arterija, itd. Mukoidi se nalaze u velikim količinama u embrionalnim tkivima, uključujući i pupčanu vrpcu novorođenčadi. Imaju zajednička fizičko-hemijska svojstva sa sluzi. Mukoidi su alkalni i, za razliku od mucina, ne precipitiraju se alkoholom ili sirćetnom kiselinom.
Mukozna degeneracija je praćena nakupljanjem sluzi i supstanci sličnih sluzi u tkivima. Postoje dvije njegove vrste: ćelijski (parenhimski) i ekstracelularni (mezenhimski).
Stanična (parenhimska) degeneracija sluzokože- poremećaji metabolizma glikoproteina u žljezdanom epitelu sluznice, koji se manifestiraju hipersekrecijom sluzi, promjenom njenog kvalitativnog sastava i smrću izlučujućih stanica.
Degeneracija sluzokože često nastaje tijekom kataralnih upalnih procesa na sluznicama kao rezultat direktnog ili indirektnog (refleksnog) djelovanja različitih patogenih podražaja. Zapažen je za bolesti probavnih, respiratornih i genitourinarnih organa.
Iritacija sluzokože uzrokuje proširenje sekrecije i povećanje intenziteta stvaranja sluzi, kao i promjenu fizičko-hemijskih svojstava i sastava same sluzi.
Histološki Degeneraciju sluzokože karakterizira hipersekrecija ili prekomjerna proizvodnja mucina u citoplazmi epitelnih (uglavnom peharastih) stanica koje oblažu sluznice, pojačano lučenje sluzi, odumiranje i deskvamacija izlučujućih stanica. Sluz može zatvoriti izvodne kanale žlijezda i uzrokovati stvaranje retencijskih cista, što je olakšano njihovim stiskanjem rastućim vezivnim tkivom. Kod rjeđeg polipoznog katara, naprotiv, uočava se hiperplazija ne samo žljezdanog, već i vezivnog tkiva.
Makroskopski sluznica je otečena, tupa, prekrivena debelim slojem sluzi, kod akutne upale organa hiperemična sa krvarenjima, a kod kronične upale zbijena zbog rasta vezivnog tkiva. Sluz proizvedena u velikim količinama, ovisno o stepenu hidratacije ili dehidracije i broju deskvamiranih stanica, različite je konzistencije i viskoznosti. Ovisno o vrsti upale organa, eksudat različitog sastava (serozni, gnojni, hemoragični) se miješa sa sluzi.
Funkcionalna vrijednost a ishod degeneracije sluzokože zavisi od intenziteta i trajanja procesa. Uz eliminaciju patogenih faktora, regeneracija epitela zbog kambijalnih ćelijskih elemenata može dovesti do potpune obnove zahvaćenih organa. Dugotrajni distrofični proces praćen je smrću ćelijskih elemenata epitela, rastom vezivnog tkiva i atrofijom žlijezda. U tim slučajevima se bilježi izražena funkcionalna insuficijencija organa (na primjer, djelomični gubitak probavne funkcije organa gastrointestinalnog trakta i kod kroničnog katara s razvojem iscrpljenosti itd.).
Posebna vrsta poremećaja metabolizma glikoproteina je koloidna distrofija (od grčkog colla - ljepilo), koju karakterizira prekomjerno stvaranje i nakupljanje koloidne mase pseudomucina u organima žlijezde (tiroidne žlijezde, bubrega, nadbubrežne žlijezde, hipofize, jajnika , sluzokože), kao i kod cistoadenoma. Fiziološki prototip koloida je tajna štitne žlijezde. Ova distrofija se javlja kod koloidne strume povezane s nedostatkom joda (endemska bolest ljudi i životinja u određenim geobiohemijskim zonama).
Mikroskopski uočava se koloidna hipersekrecija, njegovo nakupljanje u folikulima, atrofija žljezdanog tkiva, ruptura membrana i fuzija folikula sa stvaranjem cista. Novoformirani žljezdani folikuli pupanjem iz prethodnih također mogu doživjeti koloidnu degeneraciju.
Makroskopskištitna žlijezda, rjeđe drugi žljezdani organi povećavaju se u volumenu, postaju neravni sa površine, na rezu otkrivaju ciste s viskoznim ljepljivim sadržajem od sivkastožute do tamno smeđe.
Koloidna distrofija uzrokuje funkcionalno zatajenje organa. Kod koloidne strume nastaje opći mukozni edem vezivnog tkiva (miksedem).
Ekstracelularna (mezenhimalna) degeneracija sluzokože(sluz, mukozna metamorfoza) je patološki proces povezan sa nakupljanjem hromotropnih supstanci u vezivnom tkivu (vlaknastom, masnom, hrskavičnom i koštanom).
Razlozi degeneracija sluznice tkiva: iscrpljenost i kaheksija bilo koje etiologije, kao što su gladovanje, kronične bolesti (tuberkuloza, maligni tumori itd.) i disfunkcija endokrinih žlijezda (koloidna struma itd.). Suština mukozne metamorfoze sastoji se u oslobađanju kromotropne tvari (glikozaminoglikana) iz veze s proteinom i njenom nakupljanju u glavnoj tvari vezivnog tkiva.
Histološki za razliku od mukoidnog otoka, kolagena vlakna se rastvaraju i zamjenjuju masom nalik sluzi. U isto vrijeme, ćelijski elementi postaju izolirani, nabubri, poprimaju nepravilan oblik, višestruko obrađeni ili zvjezdasti, a također se otapaju.
Makroskopski zahvaćena tkiva postaju otečena, mlohava, želatinasta, impregnirana poluprozirnom masom nalik sluzi.
Funkcionalni značaj i ishod ovog procesa određuju stepen i mjesto njegovog razvoja. U početnim fazama sluzi, eliminacija uzroka praćena je obnovom strukture, izgleda i funkcije zahvaćenog tkiva.
Kako se proces razvija, dolazi do potpune likvefakcije i kolikvacione nekroze tkiva sa formiranjem šupljina ispunjenih masom nalik sluzi.
Masne degeneracije (lipidoza)
Masne distrofije (lipidoze) su morfološke promjene u tkivima povezane s poremećenim metabolizmom lipida.
Slobodna mast u ćelijama i tkivima ima oblik kapi, ponekad kristala (holesterol), rastvorljiva u organskim rastvaračima: alkohol-eter, hloroform, nerastvorljiva u vodi (za razliku od glikogena) i sirćetnoj kiselini (za razliku od proteina). Sudan III i grimizni u zamrznutim historezima fiksiranim formalinom boje crvenom, Sudan IV i osmičkom kiselinom - crnom. Nilblausulfat boji masne kiseline (lipoide) tamnoplavom, neutralnom masnoćom crvenom. Redukcija osmičke kiseline masnoćom uz formiranje osmiofilnih inkluzija omogućava je detektirati elektronskim mikroskopom. Elektronsko-mikroskopski, lipidne inkluzije se obično nalaze u obliku slobodno ležećih, neokruženih membranom, kapljicama ili kristalima (za razliku od sekretornih masnih inkluzija u žljezdanim organima, na primjer, u mliječnoj žlijezdi).
Poremećaji metabolizma lipida mogu biti ćelijski ili parenhimski (poremećaji u metabolizmu citoplazmatske masti), ekstracelularni ili stromalno-vaskularni (poremećaji metabolizma masti u masnom tkivu) i mješoviti (sistemska lipoidoza i dr.). Prema mehanizmu razvoja razlikuju: infiltraciju, transformaciju, razgradnju, odnosno dezintegraciju ćelijskih proteinsko-lipidnih kompleksa, membrana i makromolekula i izmijenjenu, odnosno "izopačenu" sintezu. Istovremeno, ne mijenja se samo kvantitativni sadržaj masti, već i njen kvalitativni sastav s pojavom proizvoda raspadanja masti.
Ćelijske (parenhimske) masne degeneracije- kršenje metabolizma citoplazmatske masti sa njenim nakupljanjem u organima i tkivima čije parenhimske ćelije inače sadrže malo slobodne masti (jetra, bubrezi), uopšte je ne sadrže (miokard, skeletni mišići, nervno tkivo itd.) ili u njima nastaje neobična mast hemijskog sastava kao rezultat patološke sinteze.
Razlozi ova distrofija: opća gojaznost, nedostatak ugljikohidrata i proteina, nedostatak lipotropnih faktora, kao što su holin, metionin, druge glukoplastične aminokiseline, vitamin B12, itd. (alipotropna, ili jednostavna, masna degeneracija). Masna degeneracija se često javlja u kombinaciji sa granularnom degeneracijom kod oboljenja metabolizma, kardiovaskularnog sistema i hematopoetskih organa (anemija, poremećaji cirkulacije), kao i kod mnogih infekcija, intoksikacija i trovanja raznim otrovima, kao što su fosfor, arsen, tetrahlorid itd. (distrofična gojaznost).
Patogeneza masna degeneracija je povezana sa infiltracijom, odnosno sa taloženjem u ćelijama masti donete protokom limfe i krvi iz gastrointestinalnog trakta, mobilizacijom masnih kiselina iz masnih depoa, kao i iz žarišta propadanja masnog tkiva. Moguća je pojačana sinteza, odnosno transformacija masti iz ugljikohidrata i bjelančevina, posebno uz njihov pretjerani unos (jednostavna gojaznost).
Najčešće se masna degeneracija razvija zbog smanjenja oksidativnih procesa i usporene asimilacije masti u patološki izmijenjenim stanicama (distrofična pretilost).
Mehanizam takve distrofične pretilosti povezan je s kršenjem oksidativnih procesa u Krebs-Embden-Meyerhof ciklusu (u mitohondrijima) zbog nedostatka kisika ili lako oksidiranih supstrata (ugljikohidrata i glukogenih aminokiselina) koji doprinose oksidaciji masnih kiselina. kiselinama i ketonskim tijelima, ili sa blokirajućim i odvajajućim djelovanjem toksičnih tvari na enzime oksidativne fosforilacije (fermentopatija).
Uz egzogenu gojaznost, izvor distrofične gojaznosti je endogena mast ćelije, koja je deo membrana, proteinsko-masni kompleksni spojevi, koji, takođe, pod uticajem navedenih razloga (hipoksija, infekcija, intoksikacija itd. ), može pretrpjeti manje ili više izraženu razgradnju, odnosno lipofanerozu (od grčkog lipos - mast, phaneros - vidljiv). Destrukcija se zasniva na enzimskim (hidrolitičkim) i fizičko-hemijskim procesima, kao što je dehidracija.
U nastanku masne degeneracije, uz njen opći mehanizam (infiltracija, transformacija, razgradnja), značajnu ulogu imaju strukturne i funkcionalne karakteristike organa i tkiva.
U jetri sa masnom infiltracijom u citoplazmi hepatocita (u njenoj perivaskularnoj zoni) isprva se pojavljuju odvojene male kapi masti (perivaskularna gojaznost malih kapi), koje se akumulacijom kreću u centar (centralna gojaznost) i spajaju se u veće kapi (gojaznost velikih kapi) i na kraju u jednu veliku kap masti; potonji gura jezgro i atrofirajuću citoplazmu na periferiju ćelije, dajući joj krikoidni oblik (slika 12), karakterističan za ćelije masnog tkiva. Masna infiltracija može biti perilobularna, centrilobularna ili difuzna.
Elektronski mikroskopski i histohemijski u jetri sa masnom infiltracijom različitog stepena (blaga, umjerena i teška), oticanjem i smanjenjem broja mitohondrija, dezintegracijom polisoma i ribozoma hepatocita, smanjenjem ili potpunim nestankom granula glikogena, smanjenjem aktivnosti redoks enzima, pojava masnih kapi u zoni negranularnog citoplazmatskog retikuluma sa manje ili više izraženom akumulacijom u hijaloplazmi. Kod razgradnje masti, radi se o lipofanerozi proteinsko-masnih kompleksnih spojeva (lipoproteina) sadržanih u zoni citoplazmatskog retikuluma uz nakupljanje liposoma, te razgradnju organela. Mitohondrije prolaze kroz masnu metamorfozu, uz formiranje citolizosoma sa povećanom aktivnošću hidrolitičkih enzima (kisela fosfataza), a zatim i lipofuscina (AV Zharov, 1975).
Sa žarišnom razgradnjom masti sa kolapsom jezgara pojavljuju se područja masne nekroze npr. u jetri, u žarištima omekšavanja mozga itd. U tim slučajevima oko takvih žarišta ili sistemski dolazi do resorptivne gojaznosti leukocita i Često se razvijaju makrofagi vezivnog tkiva iz kojih nastaju lipofagi u procesu fagocitoze masti i zrnastih kuglica. Ćelije koje fagocitiraju holesterol dobijaju lamelarni oblik. Zbog činjenice da nakupine takvih ćelija makroskopski izgledaju kao žute mrlje, nazvane su ksantomske (od grčkog xanthos - žuta).
Izgled jetre s masnom degeneracijom značajno se mijenja. Masna infiltracija perilobularnog tipa, u kombinaciji s akutnom kongestivnom hiperemijom, daje muškatni oraščić. Kod teške masne degeneracije, jetra je uvećana, žuto-smeđa, masna, mlohava, šara režnjeva je zaglađena, a na površini noža ostaje masni premaz pri rezanju. Ekstremni oblici distrofične gojaznosti jetre smanjuju gustinu organa toliko da njegovi delovi mogu da plutaju u vodi, kao što se primećuje kod mlečnih krava tokom ketoze.
U bubrezima se neutralna mast kao fiziološki fenomen javlja u epitelu interkalarnih odjeljaka tubula, Henleovih petlji i sabirnih kanala. Makroskopski, s masnom degeneracijom, bubrezi se povećavaju, dobivaju sivo-žutu boju, uzorak slojeva je zaglađen, površina reza organa je masna, ljepljiva.
Masna degeneracija miokarda manifestuje se masnom infiltracijom i razgradnjom. Masnu infiltraciju karakterizira taloženje malih kapi masti u području kapilarne i venske mreže zbog hipoksije (pretilost malih kapi). U početnoj fazi razvoja njegove male masne kapljice su orijentirane duž miofibrila, a zatim poprečna pruga nestaje, sarkozomi nabubre, sarkoplazmatski retikulum se širi, ribosomi i glikogen se raspadaju. Sa razgradnjom masti, stvaranje masti je povezano sa razgradnjom organela. Masnoća može u potpunosti zamijeniti sarkoplazmu raspadnutih vlakana (mioliza). Makroskopski, takva područja se otkrivaju u obliku sivkasto-žutih pruga, dajući miokardu uzorak tigrove kože („tigrovo srce“).
Funkcionalna vrijednost masna degeneracija parenhimskih organa i specijaliziranih elemenata drugih tkiva proizlazi iz činjenice da su funkcije organa smanjene, poremećene ili ispale. Sa očuvanjem nuklearnog aparata stanica i dijela organela citoplazme, masna degeneracija je reverzibilna. Jačanje masne nekrobioze i nekroze jezgara parenhimskih ćelija jetre, miokarda, bubrega i drugih organa praćeno je smrtnim ishodom.
Ekstracelularne (stromalno-vaskularne) masne degeneracije- metabolički poremećaji neutralnih masti i masnih kiselina u masnom tkivu, holesterola sa njegovim estrima. U patološkim stanjima, poremećaji u metabolizmu neutralne masti u masnom tkivu manifestuju se mršavošću i gojaznošću organizma.
gubitak (kaheksija)- opšte smanjenje količine masti u masnom tkivu sa manje ili više potpunim gubitkom slobodne masti u organima.
razlozi: gladovanje životinja (alimentarna distrofija), kao i kronične, iscrpljujuće, zarazne (tuberkuloza), invazivne (helmintoze) i nezarazne (gastroenteritis, bronhopneumonija, tumori, hormonski i metabolički poremećaji itd.) bolesti.
Pod mikroskopom u masnom tkivu nalaze se naborane ćelije, a u glavnoj supstanci nakupina serozne tečnosti ili supstance nalik sluzi. Manje ili više izraženi atrofični procesi (sa akumulacijom lipofuscina) nalaze se iu parenhimskim organima.
Makroskopski masno tkivo gubi masnoću, smanjuje se u volumenu, postaje mlohavo, vlažno zbog impregnacije seroznom tekućinom (serozna atrofija masti), dalje se razvija sluz tkiva (mukozna metamorfoza), poprima želatinast izgled i žućkasto-sivu boju.
Funkcionalni značaj i ishod iscrpljenost zavisi od uzroka koji ju je izazvao, mogućnosti njegovog otklanjanja i stepena patomorfoloških promjena. Početno, pa čak i klinički izraženo iscrpljenje može biti reverzibilno.
Serozna atrofija epikarda, smeđa atrofija jetre i miokarda pokazatelj su ekstremne iscrpljenosti organizma sa nepovoljnim ishodom. Kod starih životinja, posebno kod goveda i konja, ireverzibilna atrofija masti može biti praćena određenim zgušnjavanjem vlakana zbog rasta vezivnog tkiva i njegovom tamnožutom bojom zbog kondenzacije lipohroma.
Regionalno, odnosno lokalno, smanjenje količine masti u masnom tkivu naziva se lipodistrofija, koja se nalazi kod endokrinih bolesti (rekurentni ne-gnojni panikulitis i sl.) i lipogranulomatoze. Suština lipogranulomatoze je fokalna destrukcija masnog tkiva sa stvaranjem oksidirane masti, masnih cista ili upalnih granuloma. Pojava takvih žarišta povezana je s traumom, određenim zaraznim bolestima (na primjer, streptokokozom) ili potkožnim ubrizgavanjem lijekova.
Antipod iscrpljivanja je opšta gojaznost sa značajnim povećanjem masti u masnom tkivu i njenim taloženjem na neuobičajenim mestima.
razlozi: egzogeni faktori zbog prehranjenosti životinja u uslovima nedovoljne pokretljivosti i nedostatka kiseonika (alimentarna gojaznost) i endogeni faktori zbog različitih bolesti nervnog (uglavnom kod ljudi) i endokrinog sistema. Alimentarna gojaznost sa visokokaloričnom ishranom primećuje se kod svinja, muznih krava na kraju laktacije i tokom sušnog perioda, kod ovaca, ptica i mesoždera. Endokrini poremećaji praćeni gojaznošću javljaju se kod životinja s hipofunkcijom jajnika (na primjer, kod krava, mesoždera itd.), kao i drugih endokrinih žlijezda.
Mikroskopski masne naslage se nalaze izvan masnog tkiva sa stvaranjem novih masnih depoa iu unutrašnjim organima. Istovremeno, parenhimski elementi atrofiraju i u određenoj mjeri su zamijenjeni masnim tkivom. Na primjer, u intersticijumu vimena krava nastaje masno tkivo koje istiskuje sekretorno tkivo. Gojaznost epikarda i vezivnotkivnog okvira srca je praćena atrofijom mišićnih vlakana.
Makroskopski opšta gojaznost se manifestuje u manje ili više obilnim naslagama pretežno neutralne masti, ne samo u potkožnom tkivu, omentumu, mezenterijumu, ispod peritoneuma, u medijastinumu, u epikardu, već i u vezivnom tkivu takvih organa, gde je slobodno masnoća se obično javlja u malim količinama ili potpuno nedostaje. Na primjer, kako se subepikardijalna mast akumulira u obliku kontinuiranog masnog sloja, njeno taloženje se također događa u stromi organa. U takvim slučajevima srčani mišić, posebno desna strana srca, poprima mlohavu teksturu, na površini reza miokarda i ispod epikarda otkrivaju se žućkasto-bijele pruge masnog tkiva.
Opća gojaznost odnosi se na broj reverzibilnih procesa, sa izuzetkom slučajeva zbog teškog oštećenja žlijezda. Od posebnog kliničkog značaja je uključivanje srca u proces, što se manifestuje funkcionalnom insuficijencijom (miokardoza). Opća gojaznost je jedan od preduvjeta za nastanak ketoze, neplodnosti i drugih komplikacija koje su uzrok prijevremenog odstrela ili prisilnog klanja ovakvih životinja.
Lokalno nakupljanje viška masti ili lipomatoza, koji se zasniva na praznoj proliferaciji vezivnog tkiva, javlja se sa atrofijom organa (u fiziološkim uslovima sa atrofijom gušave žlezde, u patološkim stanjima - sa bubrezima, pojedinačnim limfnim čvorovima, delovima skeletnih mišića i drugim organima).
Metabolički poremećaji holesterola i njegovih estera uočeno kod kardiovaskularnih bolesti kao što su arterio- i ateroskleroza (od grč. athere - kašasta masa, skleros - zbijenost).
Savremene histohemijske i elektronske mikroskopske studije su pokazali da infiltrativnoj i resorptivnoj gojaznosti vaskularnog zida (hiperholesterolemija i lipemija) prethodi predholesterolski stadijum bolesti povezan sa poremećenim metabolizmom glikozaminoglikana i glikoproteina, plazmoragijom, mukoidnim i fibrinoidnim oticanjem ateroskokleroznog A.V. , 1965). Istovremeno, zbog povećane vaskularne permeabilnosti, ne samo da se holesterol i njegovi estri akumuliraju u intimi arterija (N. N. Anichkov, 1953), već i proteini krvne plazme: albumini, globulini, fibrinogen, b-lipoproteini i kod životinja. - pretežno neutralne masti (A. F. Tkachenko, 1965). Sve to je praćeno distrofijom i nekrozom vaskularnog zida sa stvaranjem makroskopski izraženih ateromatoznih plakova proteinsko-masnog detritusa, rastom vezivnog tkiva i njegovom hijalinozom sa sužavanjem lumena krvnih žila. U ateromatoznim plakovima kalcijeve soli najčešće ispadaju po tipu distrofične kalcifikacije ili se na njihovom mjestu pojavljuju ulcerativni defekti sa mogućim štetnim posljedicama (krvarenje, tromboza itd.).
Ugljikohidratne distrofije
Ugljikohidratne distrofije nazivaju se promjene u sastavu i količini ugljikohidrata u tkivima, zbog kršenja njihove apsorpcije, sinteze i propadanja.
Većina ugljikohidrata nalazi se u složenim spojevima stanica i tkiva. Histohemijski, polisaharidi se izoluju reakcijom sa Schiff-jodnom kiselinom (PIC ili PAS-McManusova reakcija). S obzirom da su ugljikohidrati lako rastvorljivi u vodi, za njihovu detekciju se koriste alkoholni fiksativi (Shabadash fiksator itd.). U PAS reakciji, nakon oksidacije polisaharida jodom, oslobađaju se aldehidne grupe koje daju crvene spojeve sa fuksinom Šifom (fuksin sumporna kiselina). Prema Best metodi, glikogen je obojen crvenom bojom.
U patologiji metabolizma ugljikohidrata dolazi do smanjenja ili povećanja glikogena u stanicama, kao i patološke sinteze i njegovog taloženja u organima i tkivima u kojima se normalno ne otkriva.
Razlozi: izraženo smanjenje količine glikogena u jetri, skeletnim mišićima i miokardu, uočeno kod akutnog i kroničnog gladovanja, hipoksije, groznice, hipotermije, kao i egzogenih i endogenih intoksikacija i infekcija. Nedostatak glikogena često se opaža u patologiji endokrinih žlijezda koje reguliraju njegov metabolizam. Kod Gravesove bolesti utvrđeno je smanjenje količine glikogena zbog povećanja intenziteta bazalnog metabolizma. Eksperimentalno se to kod preživača reprodukuje injekcijama tireostimulirajućeg hormona iz hipofize i tiroksina uz razvoj inducirane ketoze.
Mikroskopski kod životinja, posebno preživača, nedostatak ugljikohidrata sa smanjenjem ili nestankom rezervnog glikogena iz jetre i mišićnog tkiva često se kombinira sa granularnim
distrofija, mobilizacija masti sa povećanim stvaranjem ketonskih tijela i masnom infiltracijom parenhimskih organa, posebno jetre, bubrega i miokarda (AV Zharov, 1975). Međutim, glikogen vezan za proteine ne nestaje u potpunosti iz stanica čak ni pri potpunom izgladnjivanju. Istovremeno se bilježi patološka sinteza glikogena i njegovo taloženje u bubrezima, u epitelu uskog segmenta Henleove petlje.
Kršenja metabolizam ugljikohidrata su izraženi kod dijabetes melitusa (diabetus melitus). Njegova suština je u nedovoljnoj proizvodnji glikolitičkog hormona inzulina od strane b-ćelija Langerhansovih otočića uz razvoj degeneracije ugljikohidrata, hiperglikemije, glukozurije, poliurije, a često i komplikacija ketoze i angiopatije. Dijabetes melitus ima pankreasno (oštećenje otočnog aparata) i ekstrapankreasno (oštećenje centra za ugljikohidrate, hiperfunkcija prednje hipofize itd.) porijekla. Često se nalazi kod ljudi. Psi su bolesni, rjeđe konji i goveda. Eksperimentalni aloksan dijabetes (nakon primjene ureida aloksana ili mezooksalne kiseline) može se inducirati kod pacova, zečeva, pasa i majmuna.
Histološki kod dijabetes melitusa, uz poremećeni metabolizam glikogena u jetri i skeletnim mišićima, glikogenska infiltracija vaskularnog tkiva (dijabetička angiopatija), epitela bubrežnih tubula (zavijene i Henleove petlje), strome i vaskularnih glomerula sa razvojem bubrega primjećuje se interkapilarna dijabetička skleroza glomerula. U ovom slučaju, ponekad se glikogen oslobađa u lumen tubula.
Makroskopski organi sa ugljikohidratnom distrofijom nemaju karakteristične promjene.
Klinički uočiti funkcionalne poremećaje (ugnjetavanje, slabost srca i otežano disanje) povezane s nedostatkom energije. Štaviše, ove promjene su u početku reverzibilne. Međutim, na osnovu distrofije ugljikohidrata često je poremećen metabolizam proteina i masti, razvija se proteinska i masna distrofija, što može biti praćeno nekrozom stanica i nepovoljnim ishodom.
Povećanje količine glikogena u ćelijama organizma i njegovih patoloških naslaga nazivaju se glikogenoza.
Prekomjeran sadržaj glikogena uočava se kod anemije, leukemije, u leukocitima i ćelijama vezivnog tkiva u upaljenim žarištima, duž periferije akutnog srčanog udara ili tuberkuloznih žarišta. Glikogen se akumulira kod tovljenika, posebno kod hipofunkcije štitne žlijezde uzrokovane tireostaticima (amonijum perhlorat i dr.). Infiltracija glikogena javlja se u tkivnim elementima nekih tumora (miomi, sarkomi, karcinomi, neuromi itd.). Posebno izražena patološka infiltracija ćelija i tkiva glikogenom uočava se kod osoba sa bolestima genetski uslovljenim nedostatkom enzima glukoza-6-glikozidaze itd.
Histološki kod ovih bolesti uočava se prekomjerna akumulacija glikogena u jetri (hepatociti su „punjeni“ glikogenom), srcu, bubrezima, skeletnim mišićima, zidovima krvnih žila itd.
Makroskopski prekomjerno taloženje glikogena nema karakteristične karakteristike.
Klinički glikogenozu prati srčana i respiratorna insuficijencija, od čega dolazi do smrti (T.E. Ivanovskaya, 1989). Kod životinja ove bolesti nisu dovoljno proučavane.
Mineralne distrofije
Histopreparations.
| Tekst još nije pronađen. | |
| Infiltracijska gojaznost, atrofija miokarda |
|
| Dolazi do stanjivanja mišićnih vlakana i njihovog gubitka uzdužne ispruganosti, poprečna ispruganost se razlikuje ali ne u svim područjima. Zbog smanjenja volumena mišićnih vlakana, njihova jezgra leže bliže jedna drugoj, pa se čini da je broj jezgara u vidnom polju povećan. U izraženim slučajevima mijenja se oblik i volumen jezgara (izdužene, tamne, kao i naborane jezgre). U sakroplazmi, lipofuscin se taloži duž polova jezgara u obliku malih smećkastih granula. S razvojem atrofije, količina pigmenta se povećava, a on počinje da se taloži u sarkoplazmi kroz vlakno. U tom slučaju, sama vlakna mogu potpuno atrofirati i propasti, a na njihovom mjestu postoje gomile pigmenta. |  |
| Granularna distrofija sa nekrobiozom hepatocita |
|
| Primjećuju neravnomjerno povećanje volumena epitelnih stanica i mišićnih vlakana koja komprimiraju kapilare, oticanje i zamućenje citoplazme, glatkoću i nestanak fine strukture (četkasti rub žljezdanog epitela itd.), pojavu i nakupljanje u citoplazma malih acidofilnih zrna proteinske prirode. U isto vrijeme, granice ćelija i obrisi jezgara teško se razlikuju. Ponekad citoplazma poprima pjenasti izgled, neke ćelije se odvajaju od bazalne membrane i jedna od druge (diskompleksacija). |  |
| amiloidna distrofija |
|
| U tipičnoj općoj amiloidozi, najčešće kod domaćih životinja, amiloid ispada duž retikularnih vlakana vaskularnih i žljezdanih membrana i u periretikularne prostore parenhimskih organa (periretikularna ili parenhimska amiloidoza). Zahvaćeni su jetra, slezena, bubrezi, rjeđe nadbubrežne žlijezde, hipofiza, vlastita membrana crijevnih žlijezda, intima kapilara i arteriola. U ćelijama vezivnog tkiva nagomilavaju se preamiloidne fibrile, nestaju ribosomi, hipertrofiraju mitohondrije (gigantske mitohondrije), kao i Golgijev lamelarni kompleks. Akumulacija amiloida u tkivu je praćena atrofijom i smrću parenhimskih elemenata organa. |
 |
| Dolazi do ispiranja kalcijevih soli i djelomične resorpcije već formiranih kostiju. Resorpcija kostiju u Haversovim kanalima i drugdje provodi se enzimatski uz sudjelovanje osteoklasta uz stvaranje šupljina, odnosno lakuna (lakunarna resorpcija). Drugačija kombinacija resorpcije koštanog tkiva, smanjene sinteze novih koštanih struktura i demineralizacije dovodi u nekim slučajevima do razvoja pretežno osteoporoze, posebno kod hormonske osteodistrofije, u drugim - osteomalacije i osteofibroze sa zamjenom atrofičnog koštanog tkiva osteoidnim, hrskavičnim, vlaknaste ili masne. |  |
| U jako rastegnutim folikulima, a posebno u velikim šupljinama, žljezdani epitel izgleda kao nisko kubičan, spljošten, što ukazuje na njegovu atrofiju. Citoplazma ćelija je grubo zrnasta, jezgro je piktonsko, granice ćelija su zaglađene. Postoje folikuli u kojima je epitel zadržao svoj oblik, ali je povećan u volumenu. U citoplazmi takvih ćelija u velikom broju nalaze se mala sjajna zrnca koloida, koja ponekad ispunjavaju cijelu citoplazmu i potiskuju jezgro na periferiju stanice. uočava se i odvajanje ćelija od zidova folikula. Istovremeno s atrofičnim procesima, bilježi se hiperplazija žljezdanog epitela i stvaranje novih folikula. |  |